题目内容
同学们根据复分解反应发生的条件,并利用部分酸碱盐溶解性的信息.判断稀硫酸与如图1中的四种化合物是否能发生反应:

(1)不能与稀硫酸发生复分解反应的是 (用序号填空);
(2)试管A中产生的现象是 ;试管B中发生的反应用化学方程式表示为 ;
(3)同学们将实验后的所有物质倒入同一烧杯中,后续试验及现象如图2,综合分析可知,白色沉淀a中一定含有 ;无色滤液b中可能含有的溶质是 ;
(4)下列有关利用白色沉淀a和无色溶液b的设想中,合理的是 .
A.将无色滤液b用作钾肥
B.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色液体b
C.除去Ba(NO2)2溶液中的HNO2:向其中加入过量的白色沉淀a,然后过滤.

(1)不能与稀硫酸发生复分解反应的是
(2)试管A中产生的现象是
(3)同学们将实验后的所有物质倒入同一烧杯中,后续试验及现象如图2,综合分析可知,白色沉淀a中一定含有
(4)下列有关利用白色沉淀a和无色溶液b的设想中,合理的是
A.将无色滤液b用作钾肥
B.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色液体b
C.除去Ba(NO2)2溶液中的HNO2:向其中加入过量的白色沉淀a,然后过滤.
考点:复分解反应及其发生的条件,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:化学反应的基本类型和能量变化
分析:(1)复分解反应发生的条件是:有沉淀生成,或有水生成,或有气体生成,三个条件中,至少具备其中的一个条件,反应就能够发生;
(2)根据酸碱中和反应实质解答;
(3)根据实验现象、结合物质的水溶性等方面的情况可以判断溶液中的溶质、沉淀的成分;
(4)硫酸钾能和氯化钡反应生成白色沉淀;
除杂质时,在除去杂质的同时不能带入新的杂质.
(2)根据酸碱中和反应实质解答;
(3)根据实验现象、结合物质的水溶性等方面的情况可以判断溶液中的溶质、沉淀的成分;
(4)硫酸钾能和氯化钡反应生成白色沉淀;
除杂质时,在除去杂质的同时不能带入新的杂质.
解答:解:(1)复分解反应发生的条件是生成物中有沉淀,或气体,或水.硫酸钾与稀硫酸不能生成沉淀,或气体,或水;答案:C;
(2)试管A中开始显碱性溶液为红色,随着稀硫酸当加入碱性慢慢减弱直至消失,故溶液的红色逐渐变浅直至无色;试管B中稀硫酸与硝酸钡反应生成了硫酸钡沉淀和硝酸;答案:溶液的红色逐渐变浅直至无色;H2SO4+Ba(NO3)2═BaSO4↓+2HNO3;
(3)根据图示可知白色沉淀加入稀硝酸部分消失可知白色沉淀a中一定含有硫酸钡和碳酸钡;无色滤液b中加入过量稀硫酸无气体有无沉淀可知可能含有的溶质是硫酸钡;答案:硫酸钡、碳酸钡;硫酸钾;
(4)A.无色滤液b中可能过量的酸不能用作钾肥;
B.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色滤液b.
不合理,如果b中含有硫酸钾,取样,滴加无色滤液b时,氯化镁和氢氧化钾反应产生白色沉淀氢氧化镁,氯化钡和硫酸钾反应生成白色沉淀硫酸钡,无法鉴别.
C.除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b.合理,硫酸钡不能和硝酸反应,碳酸钡能和硝酸反应生成硝酸钡、水和二氧化碳.
答案:C;
(2)试管A中开始显碱性溶液为红色,随着稀硫酸当加入碱性慢慢减弱直至消失,故溶液的红色逐渐变浅直至无色;试管B中稀硫酸与硝酸钡反应生成了硫酸钡沉淀和硝酸;答案:溶液的红色逐渐变浅直至无色;H2SO4+Ba(NO3)2═BaSO4↓+2HNO3;
(3)根据图示可知白色沉淀加入稀硝酸部分消失可知白色沉淀a中一定含有硫酸钡和碳酸钡;无色滤液b中加入过量稀硫酸无气体有无沉淀可知可能含有的溶质是硫酸钡;答案:硫酸钡、碳酸钡;硫酸钾;
(4)A.无色滤液b中可能过量的酸不能用作钾肥;
B.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色滤液b.
不合理,如果b中含有硫酸钾,取样,滴加无色滤液b时,氯化镁和氢氧化钾反应产生白色沉淀氢氧化镁,氯化钡和硫酸钾反应生成白色沉淀硫酸钡,无法鉴别.
C.除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b.合理,硫酸钡不能和硝酸反应,碳酸钡能和硝酸反应生成硝酸钡、水和二氧化碳.
答案:C;
点评:本道考查了复分解反应的发生的条件,探究碱的性质时学生应利用学过的碱的性质并结合习题中的信息来分析解答.

练习册系列答案
相关题目
要Cu+2FeCl3=2X+CuCl2中X的化学式是( )
| A、Fe |
| B、FeCl2 |
| C、Cl2 |
| D、FeCl3 |

 自然界中存在碳氧循环,如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图回答有关问题:
自然界中存在碳氧循环,如图所示是自然界中氧气和二氧化碳的循环简图,请仔细读图回答有关问题:
 实验室需要质量分数为10%的NaCl溶液,配制质量分数为5%的氯化钠溶液.
实验室需要质量分数为10%的NaCl溶液,配制质量分数为5%的氯化钠溶液.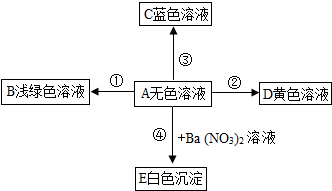
 A、B、D都是初中化学常见的氧化物,其中A、B物质的组成元素相同,C为氧气,D是形成酸雨的元凶,它们之间的相互转化关系如图所示(部分反应物、生成物及反应条件已略去).
A、B、D都是初中化学常见的氧化物,其中A、B物质的组成元素相同,C为氧气,D是形成酸雨的元凶,它们之间的相互转化关系如图所示(部分反应物、生成物及反应条件已略去).