题目内容
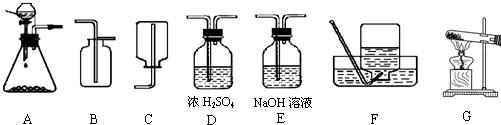
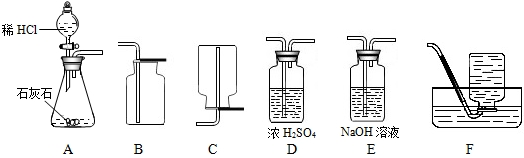
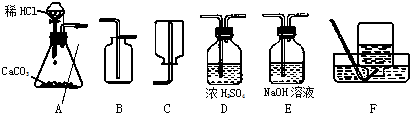
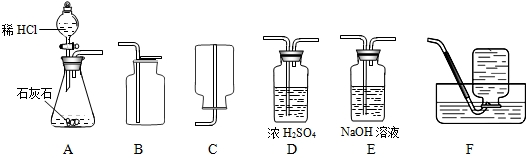
为了研究CO2的性质,需要制取并收集干燥的CO2气体,以下是老师提供的一些实验装置(提示浓硫酸具有吸水性能把气体中的水蒸气吸收而除去;NaOH溶液能和二氧化碳反应等).

(1)制取并收集干燥的CO2气体,可采用的装置组合是______(填字母).
(2)实验室制取CO2的化学方程式为______.
(3)若在上述实验中气体无法收集满,则可能的原因是______.
解:(1)A装置为制取装置,所用漏斗为分液漏斗,这种漏斗的优点是可以控制液体的滴加速度;干燥二氧化碳气体应该用D装置,利用浓硫酸的吸水性,不能用氢氧化钠溶液,因为NaOH溶液能和二氧化碳反应;收集二氧化碳气体只能用向上排空气集气法,因为二氧化碳气体密度比空气大,且能溶于水.
(2)制取书写化学方程式;
(3)实验中气体无法收集满,则可能的原因是:多种答案.
故答案为:(1)A、D、B (2)CaCO3+2HCl=CaCl2+CO2↑+H2O (3)药品量不足或气密性不好等
分析:(1)①二氧化碳的制取:固体+液体反应,不需加热,选用A装置为制取装置;②干燥的CO2气体:用D装置,利用浓硫酸的吸水性能把气体中的水蒸气吸收而除去;;③收集二氧化碳气体只能用向上排空气集气法,因为其密度比空气大,选用B装置.
(2)制取书写化学方程式:CaCO3+2HCl=CaCl2+CO2↑+H2O
(3)本小题,为开放性题目,可能的原因有多种答案.
点评:该题为实验室制取二氧化碳的一道综合题,考查二氧化碳的实验室制法原理、制取装置、收集装置的选择,以及二氧化碳的某些性质:NaOH溶液能和二氧化碳反应.
(2)制取书写化学方程式;
(3)实验中气体无法收集满,则可能的原因是:多种答案.
故答案为:(1)A、D、B (2)CaCO3+2HCl=CaCl2+CO2↑+H2O (3)药品量不足或气密性不好等
分析:(1)①二氧化碳的制取:固体+液体反应,不需加热,选用A装置为制取装置;②干燥的CO2气体:用D装置,利用浓硫酸的吸水性能把气体中的水蒸气吸收而除去;;③收集二氧化碳气体只能用向上排空气集气法,因为其密度比空气大,选用B装置.
(2)制取书写化学方程式:CaCO3+2HCl=CaCl2+CO2↑+H2O
(3)本小题,为开放性题目,可能的原因有多种答案.
点评:该题为实验室制取二氧化碳的一道综合题,考查二氧化碳的实验室制法原理、制取装置、收集装置的选择,以及二氧化碳的某些性质:NaOH溶液能和二氧化碳反应.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目