题目内容
100g某硫酸溶液与13g金属锌恰好完全反应,试计算:
(1)产生氢气多少克?
(2)这种硫酸中溶质的质量分数为多少?
解:设可制得的氢气的质量为x,反应的硫酸质量为y,
Zn+H2SO4═ZnSO4+H2↑
65 98 2
13g y x
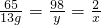
解之得:x=0.4g,y=19.6g
这种硫酸溶液的溶质质量分数为: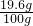 ×100%=19.6%;
×100%=19.6%;
答:(1)制得氢气0.4克;
(2)硫酸溶液的溶质质量分数是19.6%.
分析:欲正确解答本题,需根据化学方程式得出各物质之间的质量比,列出比例式,通过计算得出所需物质的质量.然后根据溶质质量分数公式计算即可.
点评:本题考查了根据化学方程式的计算,完成此题,可以依据题干提供的信息结合锌的质量进行.
Zn+H2SO4═ZnSO4+H2↑
65 98 2
13g y x
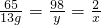
解之得:x=0.4g,y=19.6g
这种硫酸溶液的溶质质量分数为:
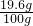 ×100%=19.6%;
×100%=19.6%;答:(1)制得氢气0.4克;
(2)硫酸溶液的溶质质量分数是19.6%.
分析:欲正确解答本题,需根据化学方程式得出各物质之间的质量比,列出比例式,通过计算得出所需物质的质量.然后根据溶质质量分数公式计算即可.
点评:本题考查了根据化学方程式的计算,完成此题,可以依据题干提供的信息结合锌的质量进行.

练习册系列答案
相关题目
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
(1)①此气体是什么物质?验证它的实验方案如下:
| 猜 想 | 验证猜想的实验步骤 | 现象及结论 |
| 我认为此气体可能是 ________ | ________ | ________ |
| 产生此气体的一个化学方程式是________ | ||
③如果用如图2所示装置收集我猜想的气体,我认为气体应从________端(填“a”或“b”)导入.
(2)100g某硫酸溶液与6.5g锌恰好完全反应,计算该硫酸溶液中溶质的质量分数?

