题目内容
6.定量测定某物质的组成是化学研究的重要内容之一,燃烧法是测定有机物元素组成的重要方法.【提出问题】某固体有机物在氧气中完全燃烧时的产物只有CO2和H2O,由此能否证明该有机物组成中只含有碳元素和氢元素?
【实验设计】为了确定该有机物的元素组成,某小组设计了如下实验(其中浓硫酸、无水CaCl2均用于吸水干燥气体;NaOH固体用于吸收CO2;部分固定装置省略).

(1)写出图中a、b两种仪器的名称:a酒精灯,b铁架台;
(2)装置A中发生反应的化学方程是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)装置B中浓硫酸的作用是吸收从A中逸出的水蒸气.
【方案评价】
(1)为了减小实验误差,C、D两盏酒精灯应先点燃D处酒精灯,待其玻璃管内的铜丝网变黑色时,再点燃C处酒精灯,由此你可以推断该小组在此实验中设计装置D的意是证明有大量氧气生成.
(2)用充有空气的储气球代替装置A,是否更利于实验的进行?否(填“是”或“否”),原因是空气中的二氧化碳会与氢氧化钠反应.
【数据处理】该小组同学在该实验中得到如下实验数据:反应前后有机物的质量减少了1.8g,装置E和F的质量分别增加了1.08g和2.64g.请你帮助他们分析该有机物的元素组成(要用计算说明).
分析 【实验设计】(1)根据仪器的作用和名称进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
(3)根据浓硫酸的吸水性回答;
【方案评价】(1)根据铜和氧气反应会生成氧化铜进行分析;
(2)根据空气中的二氧化碳会与氢氧化钠反应进行分析;
【数据处理】根据无水氯化钙会吸收水分,氢氧化钠会吸收二氧化碳进行分析.
解答 解:【实验设计】(1)图中a、b两种仪器的名称分别是铁架台,酒精灯;
(2)过氧化氢在二氧化锰的催化作用下能迅速分解生成氧气和水,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)由A处生成的氧气中含有水蒸气,浓硫酸有吸水性,可以吸收从A中溢出的水蒸气,以便进行后续实验;
【方案评价】(1)铜和氧气反应会生成氧化铜,所以待其玻璃管内的铜丝网变黑色时,再点燃C处酒精灯,由此你可以推断该小组在此实验中设计装置D的意图是:证明有大量氧气生成;
(2)空气中的二氧化碳会与氢氧化钠反应,所以不能用充有空气的储气球代替装置A;
【数据处理】无水氯化钙会吸收水分,氢氧化钠会吸收二氧化碳,所以有机物反应生成水1.08g,生成二氧化碳2.64g,
所以有机物中含有的氢元素为:$\frac{2}{18}$×1.08g=0.12g,含有的碳元素为:$\frac{12}{44}$×2.64g=0.72g,所以碳、氢元素质量为:0.12g+0.72g=0.84g,反应前后有机物的质量减少了1.8g,所以有机物的元素组成是碳、氢、氧元素.
故答案为:(1)铁架台,酒精灯;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)吸收从A中逸出的水蒸气;
方案评价】(1)黑,证明有大量氧气生成;
(2)否,空气中的二氧化碳会与氢氧化钠反应;
【数据处理】碳、氢、氧元素.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案| A. | 胶头滴管未清洗吸取和滴加不同液体 | |
| B. | 实验结束后,剩余药品都应放回原试剂瓶 | |
| C. | 给试管里的药品加热时,应先进行预热 | |
| D. | 鼻孔直接凑到容器口闻药品的气味 |
| A. | 可燃性 | B. | 气味 | C. | 颜色 | D. | 挥发性 |
| A. | 原子、分子、离子都是构成物质的微粒 | |
| B. | 氯原子和钠原子结合成氯化钠 | |
| C. | 具有稳定结构的粒子一定是稀有气体元素的原子 | |
| D. | 原子一定由质子、中子、电子构成 |
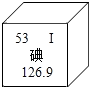 日本“3•11”大地震及其引发的海啸造成日本福岛核电站受损而释放出大量人工放射性元素碘-131(131表示原子的质量数).如图是元素周期表中碘元素的相关信息,下列说法不正确的是( )
日本“3•11”大地震及其引发的海啸造成日本福岛核电站受损而释放出大量人工放射性元素碘-131(131表示原子的质量数).如图是元素周期表中碘元素的相关信息,下列说法不正确的是( )| A. | 碘元素的元素符号是I | |
| B. | 碘元素的相对原子质量为126.9 g | |
| C. | 一个碘-131原子的原子核内有78个中子 | |
| D. | 碘元素属于非金属元素 |
| A. | 若C和D为盐和水,则该反应不一定是中和反应 | |
| B. | 此反应可能是复分解反应 | |
| C. | 若10 gA和15 gB恰好完全反应,则生成C、D的总质量为25 g | |
| D. | 若A是氧化铜、C为铜,该反应一定是置换反应 |
 A、B、X、Y、Z是初中常见的5种物质,它们有如图所示的转化关系.已知A是人体中含量最多的物质,Z是大理石的主要成分.(图中部分生成物及反应条件已略去.)
A、B、X、Y、Z是初中常见的5种物质,它们有如图所示的转化关系.已知A是人体中含量最多的物质,Z是大理石的主要成分.(图中部分生成物及反应条件已略去.)