题目内容
13.写出能实现下列反应的符号表达式并指出是化合反应还是分解反应(1)铁丝在氧气中燃烧3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4(化合反应)
(2)高锰酸钾制取氧气2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(分解反应)
(3)红磷在空气中燃烧4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5(化合反应)
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:(1)铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;该反应符合“多变一”的特征,属于化合反应.
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;该反应符合“一变多”的特征,属于分解反应.
(3)红磷在空气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;该反应符合“多变一”的特征,属于化合反应.
故答案为:(1)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;化合;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;分解;
(3)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;化合.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列图示实验操作中,正确的是( )
| A. |  加热液体 | B. |  滴加液体 | C. |  倾倒液体 | D. |  点燃酒精灯 |
18.实验室常用加热氯酸钾(KClO3)与二氧化锰(MnO2)混合物的方法制取氧气.小芳发现氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除二氧化锰(MnO2)、氧化铜(CuO)外,氧化铁(Fe2O3)也可以作氯酸钾(KClO3)分解的催化剂.
【完成实验】按下表进行实验:测定分解产生氧气的温度(分解温度越低,催化效果越好).
【分析数据、得出结论】
(1)分解所需温度越高,说明反应加热时间越长(填“长”或“短”),反应速度越慢(填“快”或“慢”)
(2)由实验① 与实验④对比,证明猜想合理;
(3)实验所用的MnO2、CuO、Fe2O3,催化效果最好的是MnO2.
【反思】(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后质量和化学性质不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证将氯酸钾与不同颗粒大小的同种催化剂等比充分混合,加热测定分解温度.
【提出猜想】除二氧化锰(MnO2)、氧化铜(CuO)外,氧化铁(Fe2O3)也可以作氯酸钾(KClO3)分解的催化剂.
【完成实验】按下表进行实验:测定分解产生氧气的温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO(质量比l:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
(1)分解所需温度越高,说明反应加热时间越长(填“长”或“短”),反应速度越慢(填“快”或“慢”)
(2)由实验① 与实验④对比,证明猜想合理;
(3)实验所用的MnO2、CuO、Fe2O3,催化效果最好的是MnO2.
【反思】(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后质量和化学性质不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证将氯酸钾与不同颗粒大小的同种催化剂等比充分混合,加热测定分解温度.
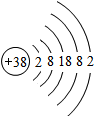 据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答:
据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答: 如图是某化工公司生产的氮肥(尿素)包装标签的部分文字,试计算:
如图是某化工公司生产的氮肥(尿素)包装标签的部分文字,试计算: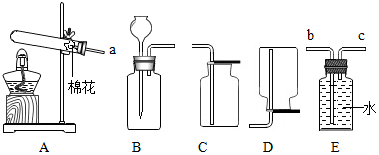 实验操作考试中为了制取氧气和二氧化碳,实验室提供了以下药品和仪器装置,请回答下列问题:
实验操作考试中为了制取氧气和二氧化碳,实验室提供了以下药品和仪器装置,请回答下列问题: