题目内容
13.钠原子和钠离子相比较,它们具有相同的( )| A. | 它们都显电性 | B. | 它们的质子数相同 | ||
| C. | 它们有相同的电子层数 | D. | 它们都具有稳定的结构 |
分析 根据钠原子和钠离子的结构进行分析.结构决定性质,钠原子失去一个电子转变为钠离子.
解答 解:由于钠原子失去一个电子转变为钠离子.所以:
A、钠原子不显电性,而钠离子带一个单位的正电荷,故A不符合题意;
B、钠原子的质子数为11,而钠离子的质子数为11,它们的质子数相同,故B符合题意;
C、钠原子的电子层数是3,钠离子的电子层数子是2.故C不符合题意;
D、钠原子的最外层电子数为1,而钠离子的最外层电子数为8,所以钠原子不具有稳定的结构,故D不符合题意.
故选B.
点评 本题考查学生利用微粒的结构来分析几个数量之间的关系,明确质子在原子核内则在反应中不发生变化,而最外层电子数决定了微粒的化学性质来解答.

练习册系列答案
相关题目
8.下列变化中与其他三种变化有着本质区别的是( )
| A. | 木头制成桌椅 | B. | 纸张被撕碎 | C. | 石蜡燃烧 | D. | 冰雪融化 |
5.有4瓶无色稀溶液分别为碳酸钠溶液、稀硫酸、氯化钡溶液和氯化钙溶液,将它们两两混合,出现的现象如下表所示:
试推断表中:A是稀硫酸,B是氯化钡溶液,C是碳酸钠溶液,D是氯化钙溶液(填名称)
试写出产生气体的化学方程式Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
| A | B | C | D | |
| A | 产生白色沉淀 | 产生无色气体 | 无明显现象 | |
| B | 产生白色沉淀 | 产生白色沉淀 | 无明显现象 | |
| C | 产生无色气体 | 产生白色沉淀 | 产生白色沉淀 | |
| D | 无明显现象 | 无明显现象 | 产生白色沉淀 |
试写出产生气体的化学方程式Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
14.下列实验操作中,正确的是( )
| A. |  塞紧橡皮塞 | B. |  滴加液体 | C. |  加热液体 | D. |  闻气味 |

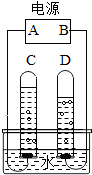 如图是简易电解水装置图,试回答问题:
如图是简易电解水装置图,试回答问题:


