��Ŀ����
�⻯�ƣ�CaH2��������һ�ִ�����ϣ���ɽ�˶�Ա����������Դ�ṩ����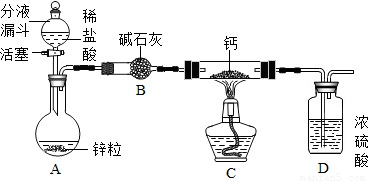
���������ϡ�
�ټ�ʯ���������ƺ��������ƵĹ������
�ڸƺ��⻯�ƶ�����ˮ��Ӧ���������������ƺ�������
���⻯�Ƶ��Ʊ���
�⻯��ͨ����������Ƽ����Ƶã�ij��ѧ��ȤС����Ƶ���ȡװ����ͼ��ʾ��ͼ�й̶�װ��ʡ�ԣ���
��1��װ��A����ȡ������Ӧ�Ļ�ѧ����ʽ�� ��
��2��װ��B�������� ��
��3��װ��D�������� ��
��4��װ��C����ȡ�⻯�ƵĻ�ѧ����ʽ�� ��
����Ʒ�ɷֵIJ��롿ͨ�����������Ƶõ��⻯����Ʒ�ijɷ����������ֲ��룺
����һ��ȫ�����⻯�ƣ� ������� ��
�����ʵ�顿����2.1g�⻯����Ʒ�������ʵ����֤������Ƿ���� ��Ҫ����������ݺͽ��ۣ���
���𰸡���������1������п�����ᷴӦ�ķ���ʽ���DZ��⣻��2�����ݼ�ʯ�ҵ���ˮ�Կ��ǣ���3������Ũ�������ˮ�Կ��ǣ���4�����ݷ���ʽ����д�������ǣ����ݷ�Ӧ���Ƿ�������ǣ������⻯����ˮ��Ӧ�����������������ǣ�
����⣺��1����Ӧ����п������д�ڵȺŵ���ߣ����������Ȼ�п��������д�ڵȺŵ��ұߣ��ù۲취��ƽ�����Է���ʽ�ǣ�Zn+2HCl=ZnCl2+H2����
��2����ʯ���������ᷴӦ��Ҳ����ˮ��Ӧ�����Լ�ʯ������������ˮ�������Ȼ������壻
��3��Ũ���������ˮ�ԣ������տ�����ˮ��������ֹ�����е�ˮ�������룬��Ʒ�Ӧ��
��4����Ӧ���Ǹƺ�����д�ڵȺŵ���ߣ����������⻯��д�ڵȺŵ��ұߣ���Ӧ�����Ǽ��ȣ����Է���ʽ�ǣ�Ca+H2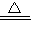 CaH2�����ڸ�Ҳ�ǹ��壬����ƹ����ˣ��⻯���л���иƣ���2.1gȫ�����⻯��������������ΪX��
CaH2�����ڸ�Ҳ�ǹ��壬����ƹ����ˣ��⻯���л���иƣ���2.1gȫ�����⻯��������������ΪX��
CaH2+2H2O�TCa��OH��2+2H2����
42 4
2.1g X
����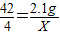 ���X=0.2g������ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g��������������
���X=0.2g������ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g��������������
�ʴ�Ϊ����1��Zn+2HCl=ZnCl2+H2������2������ˮ�������Ȼ������壻��3�����տ����е�ˮ��������ֹ�����е�ˮ�������룬��Ʒ�Ӧ����4��Ca+H2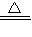 CaH2 ����������⻯�ƺƣ������ʵ�顿ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g��������������
CaH2 ����������⻯�ƺƣ������ʵ�顿ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g��������������
���������ʱע�������Ŀ������Ϣ�������ѧ֪ʶ������Ϣ�������ϣ���������������⡢������⣮
����⣺��1����Ӧ����п������д�ڵȺŵ���ߣ����������Ȼ�п��������д�ڵȺŵ��ұߣ��ù۲취��ƽ�����Է���ʽ�ǣ�Zn+2HCl=ZnCl2+H2����
��2����ʯ���������ᷴӦ��Ҳ����ˮ��Ӧ�����Լ�ʯ������������ˮ�������Ȼ������壻
��3��Ũ���������ˮ�ԣ������տ�����ˮ��������ֹ�����е�ˮ�������룬��Ʒ�Ӧ��
��4����Ӧ���Ǹƺ�����д�ڵȺŵ���ߣ����������⻯��д�ڵȺŵ��ұߣ���Ӧ�����Ǽ��ȣ����Է���ʽ�ǣ�Ca+H2
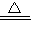 CaH2�����ڸ�Ҳ�ǹ��壬����ƹ����ˣ��⻯���л���иƣ���2.1gȫ�����⻯��������������ΪX��
CaH2�����ڸ�Ҳ�ǹ��壬����ƹ����ˣ��⻯���л���иƣ���2.1gȫ�����⻯��������������ΪX��CaH2+2H2O�TCa��OH��2+2H2����
42 4
2.1g X
����
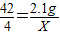 ���X=0.2g������ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g��������������
���X=0.2g������ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g���������������ʴ�Ϊ����1��Zn+2HCl=ZnCl2+H2������2������ˮ�������Ȼ������壻��3�����տ����е�ˮ��������ֹ�����е�ˮ�������룬��Ʒ�Ӧ����4��Ca+H2
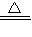 CaH2 ����������⻯�ƺƣ������ʵ�顿ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g��������������
CaH2 ����������⻯�ƺƣ������ʵ�顿ȡ2.1 g��Ʒ������ˮ��Ӧ���ռ���Ӧ���ɵ������������ɵ�������������0.2 g�������������������������������С��0.2 g�����������������������ʱע�������Ŀ������Ϣ�������ѧ֪ʶ������Ϣ�������ϣ���������������⡢������⣮

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ

