题目内容
铜是人类最早利用的金属之一。
(1)下列铜制品中,利用金属导热性的是 (填字母序号)。

(2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为 。
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去):

已知:2Cu+2H2SO4 +O2
+O2 2CuSO4+2H2O
2CuSO4+2H2O
①过程Ⅱ中分离操作的名称是 。
②过程Ⅲ中有气体产生,反应的化学方程式为 。
③A~E中含铜、锌两种元素的物质有 (填字母序号)。
本题主要考查金属的性质及用途;过滤的原理、方法及其应用。
(1)利用铜的导热性可以做成火锅。(2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,反应的化学方程式为Fe+CuSO4====FeSO4+Cu。(3)由题意可知,含Cu、Zn的电池铜帽与稀硫酸和氧气反应生成了硫酸铜 和硫酸锌的混合液A,根据实验的目的,为了得到铜和硫酸锌,应向A溶液中加入过量的锌,通过过滤得到了硫酸锌溶液和铜锌的固体混合物C,为了得到铜和硫酸锌,应向C中加入稀硫酸,所以:①过程Ⅱ中为了分离固体和液体,操作的名称是过滤;②过程Ⅲ中是稀硫酸与锌反应生成了硫酸锌和氢气,反应的化学方程式是Zn+H2SO4====ZnSO4+H2↑;③由上述分析可知,溶液A是硫酸铜和硫酸
和硫酸锌的混合液A,根据实验的目的,为了得到铜和硫酸锌,应向A溶液中加入过量的锌,通过过滤得到了硫酸锌溶液和铜锌的固体混合物C,为了得到铜和硫酸锌,应向C中加入稀硫酸,所以:①过程Ⅱ中为了分离固体和液体,操作的名称是过滤;②过程Ⅲ中是稀硫酸与锌反应生成了硫酸锌和氢气,反应的化学方程式是Zn+H2SO4====ZnSO4+H2↑;③由上述分析可知,溶液A是硫酸铜和硫酸 锌的混合物,固体C是铜和锌的混合物,所以,含铜、锌两种元素的物质有A、C。
锌的混合物,固体C是铜和锌的混合物,所以,含铜、锌两种元素的物质有A、C。
答案:(1)C (2)Fe+CuSO4====FeSO4+Cu
(3)①过滤 ②Zn+H2SO4====ZnSO4+H2↑
③A、C

练习册系列答案
相关题目
 铜质奖牌 B.
铜质奖牌 B. 铜导线 C.
铜导线 C. 铜火锅
铜火锅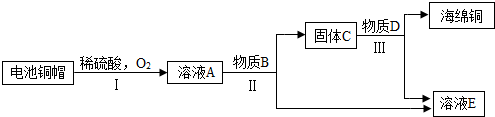


 2CuSO4+2H2O
2CuSO4+2H2O 

 2CuSO4+2H2O
2CuSO4+2H2O


