题目内容
18. 请回答:胃酸的主要成分是盐酸,胃酸过多会引起胃痛.右图是一种治疗胃病药物的标签.
请回答:胃酸的主要成分是盐酸,胃酸过多会引起胃痛.右图是一种治疗胃病药物的标签.(1)该药物的主要作用是中和胃液中过多的盐酸,这种药物在胃中发生反应的化学方程式是Al(OH)3+3HCl=AlCl3+3H2O.
(2)胃痛时吃几块苏打饼干(含纯碱)可减轻胃痛,该反应的化学方程式是:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
分析 本题根据信息可知考查酸的化学性质,胃酸的主要成分是盐酸,胃酸过多会引起胃痛,由酸能与碱、与盐反应的性质可知应服用能与酸反应的药物.
解答 解:(1)该药物的有效成分是氢氧化铝,能与盐酸反应,故答案为:中和胃液中过多的盐酸;Al(OH)3+3HCl=AlCl3+3H2O;
(2)苏打饼干中含纯碱,纯碱能与盐酸反应生成二氧化碳和水而使胃酸减少,从而减轻胃痛,故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 本题在考查酸的化学性质的同时,利用化学知识解决了生活中的问题,具有很强的实际应用性,但应注意具体问题具体分析,对于胃穿孔的病人不能服用含纯碱的药物.

练习册系列答案
相关题目
20.下表中,除去物质所含少量杂质的方法正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | 氯化钠溶液 | 氯化镁 | 加适量烧碱溶液再过滤 |
| B | 铁粉 | 铜粉 | 滴加适量稀盐酸,过滤 |
| C | 一氧化碳气体 | 二氧化碳气体 | 点燃 |
| D | 氢氧化钠溶液 | 氢氧化钙 | 加入过量碳酸钠充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
6. 据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.同学们对废旧手机中的金属回收产生兴趣.
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.同学们对废旧手机中的金属回收产生兴趣.
【提出问题】从废旧手机中可以回收到哪些有价值的金属?如何回收?
【查阅资料】
i.手机电路板中的金属及其价格如下表所示:
说明:Fe、Cu、Al、Ni的含量用质量分数(%)表示,Au、Ag、Pd的含量的单位为“g/t”.
ii.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后; NiCl2溶液为绿色.
Iii. 2Cu+O2+2H2SO4 2CuSO4+2H2O
【实验方案】
第一步:选择值得回收的金属.
依据资料i中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,原因是:①
它们的市场价格较高;②Au、Ag、Cu、Pd在收集电路板中的含量高于其在矿石中的含量.
第二步:设计实验分离、回收部分金属.
【问题讨论】
(1)由步骤I中的现象,可推知的焊锡的物理性质是熔点较低.
(2)步骤II对应的实验现象是溶液变成绿色,有无色气泡产生.
(3)步骤II所得溶液中,一定含有的金属元素是Fe、Al、Ni.
(4)步骤V的操作是向IV中得到的滤液中加入铁片.
【反思交流】
为了确认步骤IV中滤纸上的金属成分,应进一步查阅的资料为Au、Ag、Pd在加热条件下,能否与氧气、稀硫酸发生反应.
 据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.同学们对废旧手机中的金属回收产生兴趣.
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.同学们对废旧手机中的金属回收产生兴趣.【提出问题】从废旧手机中可以回收到哪些有价值的金属?如何回收?
【查阅资料】
i.手机电路板中的金属及其价格如下表所示:
| 种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
| 市场价格($/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
| 矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
| 手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
ii.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后; NiCl2溶液为绿色.
Iii. 2Cu+O2+2H2SO4 2CuSO4+2H2O
【实验方案】
第一步:选择值得回收的金属.
依据资料i中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,原因是:①
它们的市场价格较高;②Au、Ag、Cu、Pd在收集电路板中的含量高于其在矿石中的含量.
第二步:设计实验分离、回收部分金属.
| 序号 | 实验步骤 | 实验现象 |
| I | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
| II | 将金属电路放入烧杯中,加入足量稀盐酸浸泡 | 溶液变成绿色,有无色气泡产生 |
| III | 取II中未溶解的金属电路,用蒸馏水洗净后,放入如右图所示装置中,进行实验.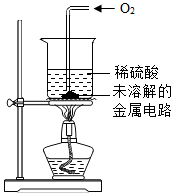 | 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
| IV | 过滤III中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
| V | 向IV中得到的滤液中加入铁片 | 得到红色固体 |
(1)由步骤I中的现象,可推知的焊锡的物理性质是熔点较低.
(2)步骤II对应的实验现象是溶液变成绿色,有无色气泡产生.
(3)步骤II所得溶液中,一定含有的金属元素是Fe、Al、Ni.
(4)步骤V的操作是向IV中得到的滤液中加入铁片.
【反思交流】
为了确认步骤IV中滤纸上的金属成分,应进一步查阅的资料为Au、Ag、Pd在加热条件下,能否与氧气、稀硫酸发生反应.
3.下列说法正确的是( )
| A. | 铁比铝更易生锈,所以铁比铝活泼 | B. | 用烧碱改良酸性土壤 | ||
| C. | 有盐和水生成的反应都是中和反应 | D. | 铁丝在氧气中燃烧生成四氧化三铁 |
 A、B、C、D、E、F是初中化学中常见物质,且均含有一种相同元素,其中A为单质,B、C、E为氧化物,且E过多会引起温室效应,F是一种钙盐,它们之间的关系如图所示,(图中“-”表示两端物质能发生化学反应,“→”表示物质转化关系)
A、B、C、D、E、F是初中化学中常见物质,且均含有一种相同元素,其中A为单质,B、C、E为氧化物,且E过多会引起温室效应,F是一种钙盐,它们之间的关系如图所示,(图中“-”表示两端物质能发生化学反应,“→”表示物质转化关系)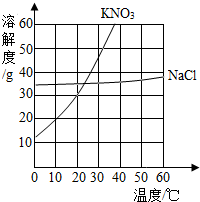 如图,根据KNO3和NaCl的溶解度曲线,回答下列问题:
如图,根据KNO3和NaCl的溶解度曲线,回答下列问题: 测定空气中氧气所占的体积分数,某同学设计了如图密闭装置中实验,在一个耐热活塞的底部放一小块(足量)白磷(白磷40℃时就能燃烧),然后迅速将活塞下压,可以观察到的现象为白磷燃烧起来,产生大量白烟;冷却至原来温度时,慢慢松开手,活塞最终将回到刻度4处,由此实验可以得出的结论是氧气体积约占空气体积的五分之一.其中磷燃烧的文字表达式为磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
测定空气中氧气所占的体积分数,某同学设计了如图密闭装置中实验,在一个耐热活塞的底部放一小块(足量)白磷(白磷40℃时就能燃烧),然后迅速将活塞下压,可以观察到的现象为白磷燃烧起来,产生大量白烟;冷却至原来温度时,慢慢松开手,活塞最终将回到刻度4处,由此实验可以得出的结论是氧气体积约占空气体积的五分之一.其中磷燃烧的文字表达式为磷+氧气$\stackrel{点燃}{→}$五氧化二磷. 如图所示.
如图所示.