题目内容
8.下列关于物质的用途不正确的是( )| A. | 在医疗上用碳酸氢钠来治疗胃酸过多 | |
| B. | 用加了洗涤剂的水来清洗油污 | |
| C. | 商家用甲醛水溶液(福尔马林)浸泡海产品来延长海产品的保质期 | |
| D. | 有些净水器利用活性炭来吸附、过滤水中的杂质 |
分析 A.根据碳酸氢钠与胃液中的盐酸反应生成氯化钠、水和二氧化碳进行分析;
B.根据洗涤剂具有乳化作用分析;
C.根据甲醛能破坏蛋白质的结构进行分析;
D.根据活性炭具有吸附性进行分析.
解答 解:A.碳酸氢钠与胃液中的盐酸反应NaHCO3+HCl=NaCl+H2O+CO2↑,碳酸氢钠碱性弱可用于治疗胃酸(主要成分是盐酸)过多,故A正确;
B.洗涤剂具有乳化作用,可用加了洗涤剂的水来清洗油污,故B正确;
C.甲醛有毒,能破坏人体蛋白质的结构,使蛋白质变质,不能用甲醛水溶液浸泡海产品,故C错误;
D.活性炭具有吸附性,能吸附水中的色素和异味,所以可用于净水器中用来吸附、过滤水中杂质,故D正确;
故选C.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.实验探究一:课本第二单元课后作业中有“寻找新的催化剂”的探究内容,实验中学探究小组据此设计了如下探究方案.
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
【拓展应用】
己知CuSO4也可作为过氧化氢分解的催化剂.向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气3.2g.
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质.淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究.
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质.写出KOH变质的化学方程式为2KOH+CO2═K2CO3+H2O.
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想1不成立.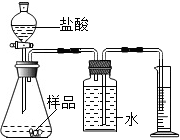
(2)准确称取一定质量的固体样品,放在如图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由不可行,因为二氧化碳能够溶于水,并且能和水反应生成碳酸.
(3)请你另外设计一个方案,进一步探究变质情况
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
| 实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ.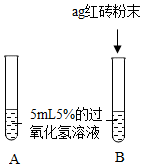 | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是氧气 ②红砖粉末能改变过氧化氢分解速率 |
| Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的质量和化学性质在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ.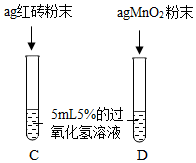 | 两试管中均产生气泡且加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的快 | 红砖粉末的催化效果没有二氧化锰粉末好 |
己知CuSO4也可作为过氧化氢分解的催化剂.向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气3.2g.
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质.淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究.
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质.写出KOH变质的化学方程式为2KOH+CO2═K2CO3+H2O.
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想1不成立.

(2)准确称取一定质量的固体样品,放在如图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由不可行,因为二氧化碳能够溶于水,并且能和水反应生成碳酸.
(3)请你另外设计一个方案,进一步探究变质情况
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品于试管中,加入足量水溶解,加入足量的氯化钙溶液,静置后滴加酚酞试液 | 产生白色沉淀,溶液变红色 | 猜想2成立 |
19.欲配制10.0%的NaCl溶液50g,部分操作如下图所示,正确的是( )
| A. |  取固体 | B. |  称固体 | C. |  量取水 | D. |  写标签 |
16.如图是某反应的微观示意图,下列有关该反应的说法不正确的是( )

| A. | 属于置换反应 | |
| B. | 相对分子质量最小的是NH3 | |
| C. | 生成丙和丁的质量比为1:3 | |
| D. | 氢元素的化合价在反应前后没有变化 |
13.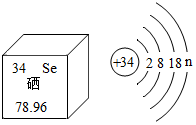 亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )
亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )
 亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )
亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )| A. | Na2SeO3中Se化合价为+4 | B. | n的值为6 | ||
| C. | Se是一种金属元素 | D. | Se的相对原子质量为78.96 |
20. 甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法不正确的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法不正确的是( )
 甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法不正确的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | t1℃时,甲和丙的溶解度都为20g | |
| B. | 甲的溶解度一定大于乙的溶解度 | |
| C. | 采用冷却结晶的方法可以分离甲中混有的少量的丙 | |
| D. | t2℃时,将70克甲放入100克水中,充分溶解后,所得到溶液为饱和溶液,且溶液的总质量为150克 |
17.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X→盐+Y”这种表达式进行整理,下列小明的观点错误的是( )
| 选项 | X的物质类别 | 观点描述 |
| A | 金属 | 若X为Cu,则反应能够发生 |
| B | 金属氧化物 | 若X为MgO,则Y为H2O |
| C | 碱 | 若X为NaOH,则盐为Na2SO4 |
| D | 盐 | 若X为BaCl2,则生成白色沉淀 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |


 “阴阳师”是最近一款非常风靡的手游.有一天小薇在画符召唤式神的时候发现,初中化学常见的5种物质也符合符咒上的五角星关系.已知A、C、E均为氧化物,A是人体呼吸作用的主要产物;在实验室中B可以用来制取A,而D的溶液可以用来检验A;C和E反应能生成D.相互之间连线表示能发生化学反应.则
“阴阳师”是最近一款非常风靡的手游.有一天小薇在画符召唤式神的时候发现,初中化学常见的5种物质也符合符咒上的五角星关系.已知A、C、E均为氧化物,A是人体呼吸作用的主要产物;在实验室中B可以用来制取A,而D的溶液可以用来检验A;C和E反应能生成D.相互之间连线表示能发生化学反应.则