题目内容
2.金属锂(元素符号为Li)在通讯和航天领域中具有及其重要的用途.它的化合物氢氧化锂(LiOH)是一种易溶于水的白色固体,有辣味,具有强碱性和腐蚀性.载人航天飞船中通常用LiOH代替NaOH来吸收航天员呼吸产生的CO2.“神舟10号”于2013年6月11日发射升空,于26日成功返回着陆.请回答下列问题:
(1)在物质分类中氢氧化锂属于碱(填“酸”“碱”或“盐”).
(2)试写出LiOH和CO2反应的化学方程式:CO2+2LiOH═Li2CO3+H2O.
(3)假设飞船返回穿越大气层时,有一段为匀速降落过程,则在此过程中飞船动能不变(填“不变”“增大”或“减小”,下同),势能减小.
分析 (1)氢氧化锂是由锂粒子和氢氧根离子构成的化合物,进行分析解答.
(2)LiOH和CO2反应生成碳酸锂和水,进行分析解答.
(3)动能大小的影响因素:质量、速度,质量越大、速度越快,动能越大;质量越大,高度越高,重力势能越大.
解答 解:(1)氢氧化锂是由锂粒子和氢氧根离子构成的化合物,属于碱.
(2)LiOH和CO2反应生成碳酸锂和水,反应的化学方程式为:CO2+2LiOH═Li2CO3+H2O.
(3)假设飞船返回穿越大气层时,有一段为匀速降落过程,则在此过程中速率不变,则飞船动能不变;由于是降落过程,高度逐渐下降,势能减小.
故答案为:(1)碱;(2)CO2+2LiOH═Li2CO3+H2O;(3)不变;减小.
点评 本题难度不大,掌握碱的化学性质、酸碱盐的特征、动能与重力势能的影响因素是正确解答本题的关键.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
13.秦山核电基地是中国核电机组数量最多、堆型最丰富,装机最大的核电基地,其获得核能的途径是( )
| A. | 轻核的裂变 | B. | 重核的聚变 | C. | 轻核的聚变 | D. | 重核的裂变 |
14.下列各组现象属于化学变化的是( )
| A. | 蜡烛熔化 | B. | 铁锅生锈 | C. | 电灯发光 | D. | 汽油挥发 |
17.白蚁能分泌蚁酸,蚁酸的化学性质与盐酸相似,能腐蚀多种物质.下列做难被蚁酸腐蚀的是( )
| A. | 铜制塑像 | B. | 镀锌水管 | C. | 大理石栏杆 | D. | 铝合金门窗 |
7.下列做法符合“美丽北海,清洁城乡”活动主题的是( )
| A. | 生活垃圾分类处理 | B. | 直接焚烧秸杆 | ||
| C. | 任意排放生活污水 | D. | 塑料袋随地丢弃 |
14.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表
关于此反应,下列认识正确的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 5 | 2 | 42 | 12 |
| 反应后质量(g) | X | 2 | 6 | 40 |
| A. | 乙一定是催化剂 | |
| B. | 参加反应的丙、丁的质量比为1:2 | |
| C. | X的值为13 | |
| D. | 乙、丙中所含元素种类与甲、丁中所含元素种类相同 |
10.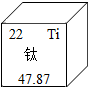 钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )
钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )
 钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )
钛和钛合金是21世纪的重要材料,具有很多优良性能,钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见图,下列说法中错误的是( )| A. | 钛元素原子的质子数为22 | B. | 钛元素的相对原子质量为47.87 | ||
| C. | 钛元素属于非金属元素 | D. | 钛原子核外共有22个电子 |