题目内容
配制溶质质量分数一定的氯化钠溶液常按如图操作顺序进行.
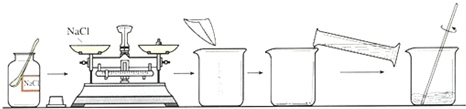
请回答下列问题:
(1)计算配制100g溶质质量分数为5%的氯化钠溶液所需:氯化钠 g,水 g.
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 .
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 .
(4)在用量筒量取所需水的过程中,小明俯视读数,这样配得的溶液浓度会 (填“偏高”、“偏低”、或“无影响”).

请回答下列问题:
(1)计算配制100g溶质质量分数为5%的氯化钠溶液所需:氯化钠
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是
(4)在用量筒量取所需水的过程中,小明俯视读数,这样配得的溶液浓度会
考点:一定溶质质量分数的溶液的配制,称量器-托盘天平
专题:溶液、浊液与溶解度
分析:(1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品.
(3)根据配制溶质质量分数一定的溶液的步骤分析解答玻璃棒的作用;
(4)根据俯视读数看到的读数偏大,但量取的液体正好偏小,根据溶质不变,溶剂减少,溶液质量就减少来判断溶质质量分数的情况.
(2)使用托盘天平称量药品时应遵循“左物右码”,称量过程中他发现指针偏左了,说明药品质量大于砝码质量,应减少药品.
(3)根据配制溶质质量分数一定的溶液的步骤分析解答玻璃棒的作用;
(4)根据俯视读数看到的读数偏大,但量取的液体正好偏小,根据溶质不变,溶剂减少,溶液质量就减少来判断溶质质量分数的情况.
解答:解:
(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-5g=95g.
(2)用托盘天平称量5g固体药品NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl.
(3)配制100g溶质质量分数为5%的氯化钠溶液,玻璃棒在该实验中所起的作用是搅拌,加速固体溶解;
(4)用量筒量取水时俯视读数,所量的水偏少,所得溶液中氯化钠的质量分数会偏大.
答案:
(1)5;95;(2)B;(3)搅拌,加速固体溶解;(4)偏高
(1)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-5g=95g.
(2)用托盘天平称量5g固体药品NaCl时,步骤是:调节天平平衡,在右盘上加砝码和拨动游码,然后向左边托盘添加药品直至天平平衡;称量过程中他发现指针偏左了,说明NaCl的质量大于砝码质量,应减少NaCl.
(3)配制100g溶质质量分数为5%的氯化钠溶液,玻璃棒在该实验中所起的作用是搅拌,加速固体溶解;
(4)用量筒量取水时俯视读数,所量的水偏少,所得溶液中氯化钠的质量分数会偏大.
答案:
(1)5;95;(2)B;(3)搅拌,加速固体溶解;(4)偏高
点评:本题难度不大,明确一定溶质质量分数溶液的配制的步骤、所需仪器、注意事项等是正确解答此类题的关键.

练习册系列答案
相关题目
钛和钛合金被认为是21世纪的重要金属材料,下列理由不恰当的是( )
| A、熔点高 密度小 |
| B、可塑性好,易于加工,机械性能好 |
| C、抗腐蚀性能好 |
| D、具有形状记忆 |
已知R元素的相对原子质量为M,若R2+核外有x个电子,则R的原子核内的中子数为( )
| A、M-x+2 |
| B、M+x+2 |
| C、M-x-2 |
| D、M+x-2 |
