题目内容
鸡蛋壳的主要成分是碳酸钙.某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如下图所示(忽略水蒸气的挥发),其中当反应进行到B点时,恰好完全反应.请计算(计算结果保留1位小数):(1)产生CO2的质量为______g;
(2)该鸡蛋壳中CaCO3的质量分数.

【答案】分析:(1)分析题中反发生的变化可知,由于二氧化碳气体的放出变化后烧杯中的反应剩余物的质量减小,减小的质量即放出二氧化碳气体的质量;
(2)根据反应的化学方程式,由生成二氧化碳的质量计算参加反应的碳酸钙的质量,使用质量分数计算公式求出鸡蛋壳中CaCO3的质量分数;
解答:解:(1)根据质量守恒定律,结合图象的数值可知生成二氧化碳的质量=95g-90.6g=4.4g;
(2)设该鸡蛋壳中CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
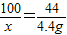
x=10g
该鸡蛋壳中CaCO3的质量分数=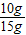 ×100%≈66.7%
×100%≈66.7%
故答案为:(1)4.4;(2)答:该鸡蛋壳中CaCO3的质量分数约为66.7%;
点评:根据质量守恒定律:石灰石与稀盐酸反应,反应前后减少的质量为二氧化碳的质量,知识解决此题的关键;
(2)根据反应的化学方程式,由生成二氧化碳的质量计算参加反应的碳酸钙的质量,使用质量分数计算公式求出鸡蛋壳中CaCO3的质量分数;
解答:解:(1)根据质量守恒定律,结合图象的数值可知生成二氧化碳的质量=95g-90.6g=4.4g;
(2)设该鸡蛋壳中CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
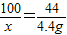
x=10g
该鸡蛋壳中CaCO3的质量分数=
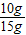 ×100%≈66.7%
×100%≈66.7%故答案为:(1)4.4;(2)答:该鸡蛋壳中CaCO3的质量分数约为66.7%;
点评:根据质量守恒定律:石灰石与稀盐酸反应,反应前后减少的质量为二氧化碳的质量,知识解决此题的关键;

练习册系列答案
相关题目