题目内容
15.下列实验现象的描述中,正确的是( )| A. | 镁条在空气中燃烧,发出耀眼的强光,生成氧化镁 | |
| B. | 铁丝在氧气中燃烧时,火星四射,生成黑色固体 | |
| C. | 红磷在空气中燃烧产生大量的白雾 | |
| D. | 木炭在氧气中燃烧,生成有刺激性气味的气体 |
分析 A、根据镁条在空气中燃烧的现象进行分析判断.
B、根据铁丝在氧气中燃烧的现象进行分析判断.
C、根据红磷在空气中燃烧的现象进行分析判断.
D、根据木炭在氧气中燃烧的现象进行分析判断.
解答 解:A、镁条在空气中燃烧,发出耀眼的强光,生成氧化镁是实验结论而不是实验现象,故选项说法错误.
B、铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体,故选项说法正确.
C、红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
D、木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的无色、无味的气体,故选项说法错误.
故选:B.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象时,需要注意光和火焰、烟和雾、实验结论和实验现象的区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5. 化学兴趣小组的同学对“影响金属与稀盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与稀盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应的剧烈程度受哪些因素的影响?
【做出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用的金属均已用砂纸打磨.
实验(1)为探究猜想a,小明同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,请写出放锌片的试管中发生反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
从实验现象可以判断:金属活动性Zn>Fe(填“>”“<”或“=”).
【得出结论1】:金属活动性越强,反应的程度越剧烈.
实验(2)为探究猜想b,小组同学设计如图装置进行实验,所用药品、实验数据如下表:
其中注射器的作用是测量生成气体的体积.
【得出结论2】:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是盐酸的浓度越大,反应越剧烈.
【反思评价】
根据表中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因锌与盐酸反应产生气体的速率先逐渐加快,后变慢,因为锌与盐酸是放热反应,所以开始时反应较慢,随温度升高,产生气体速率加快,随着反应的进行,盐酸不断被消耗,浓度降低,产生气体速度变慢. 通过以上探究,你认为金属与盐酸反应的剧烈程度还可能受哪些因素影响?固体的表面积(或形状)或反应的温度或金属的纯度等(合理即可)(写一条即可).
 化学兴趣小组的同学对“影响金属与稀盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与稀盐酸反应的剧烈程度的因素”进行了探究.【提出问题】金属与盐酸反应的剧烈程度受哪些因素的影响?
【做出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用的金属均已用砂纸打磨.
实验(1)为探究猜想a,小明同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,请写出放锌片的试管中发生反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
从实验现象可以判断:金属活动性Zn>Fe(填“>”“<”或“=”).
【得出结论1】:金属活动性越强,反应的程度越剧烈.
实验(2)为探究猜想b,小组同学设计如图装置进行实验,所用药品、实验数据如下表:
其中注射器的作用是测量生成气体的体积.
| 实验编号 | 选用金属 (均取2g) | 盐酸浓度 (均取50ml) | 每分钟产生气体的体积/ml | |||||
| 1分钟 | 1~2分钟 | 2~3分钟 | 3~4分钟 | 4~5分钟 | 前5分钟共收集气体的总体积/mL | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【反思评价】
根据表中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因锌与盐酸反应产生气体的速率先逐渐加快,后变慢,因为锌与盐酸是放热反应,所以开始时反应较慢,随温度升高,产生气体速率加快,随着反应的进行,盐酸不断被消耗,浓度降低,产生气体速度变慢. 通过以上探究,你认为金属与盐酸反应的剧烈程度还可能受哪些因素影响?固体的表面积(或形状)或反应的温度或金属的纯度等(合理即可)(写一条即可).
6.如图是对四个实验绘制的图象,其中实验结果与图象正确的是( )
| A. | 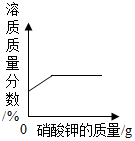 某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体 | |
| B. | 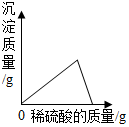 将稀硫酸滴入一定量的BaCl2溶液中 | |
| C. | 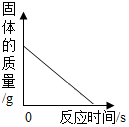 将一定质羹的石灰石加入试管中充分高温煅烧 | |
| D. | 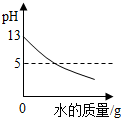 向pH为13的NaOH溶液中加水稀释 |
3.下列实验操作,不能达到预期目的是( )
| A. | 用10 mL量筒量取8.2 mL水 | |
| B. | 用托盘天平称取5.60 g氧化铜粉末 | |
| C. | 用排水集气法可得到比较纯净的氧气 | |
| D. | 用过滤的方法可以除去水中所有的杂质 |
10.下列图示的实验操作正确的是( )
| A. |  氧气验满 | B. |  称取NaCl 称取NaCl | C. |  稀释浓硫酸 | D. |  取用药品 |
7.一种物质在氧气中燃烧,生成物中只有水和二氧化碳,则此物质是( )
| A. | 一定含碳氧两种元素 | B. | 一定含碳氢两种元素 | ||
| C. | 一定含碳氢氧三种元素 | D. | 不能确定 |

 表示的是Al3+(填离子符号).
表示的是Al3+(填离子符号). 水是一种重要的资源.
水是一种重要的资源.