题目内容
17.已知X、Y、Z分别是金属活动性顺序中的三种金属,并能发生下列化学反应,①X+YSO4═XSO4+Y
②X+H2SO4═XS04+H2↑
③Y+2ZN03═Y(NO3)2+2Z
④Z+H2SO4,不发生反应
其中不符合上述规律的三种金属组合是( )
| A. | Mg、Fe、Ag | B. | Zn、Fe、Cu | C. | Al、Zn、Hg | D. | Fe、Cu、Ag |
分析 在金属活动性顺序中,氢前的金属能置换出酸中的氢,位置越靠前,反应的越剧烈,位置在前的金属能把位于其后的金属从其盐溶液中置换出来;然后根据①②③④中的反应情况推测各金属之间的活动性,根据化学式推断化合价.
解答 解:由①可以得出,活动性X>Y,并且由YSO4和XSO4,可知X、Y在化合物中都显+2价,所以C错误;由②可以得出,X活动性>H;由③可以得出,活动性Y>Z,并且由ZN03,可知Z在化合物中都显+1价,选项B错误,由④可以得出,活动性H>Z;所以BC不符合题意.
故选BC.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义以及金属活动性顺序结合化合价进行.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
7.实验操作考查,小松同学抽到“蒸发8mL食盐水至结晶”的考题,该实验不需要使用的仪器是( )
| A. |  试管 | B. |  蒸发皿 | C. |  酒精灯 | D. |  量筒 |
5.甲烷和水反应制备水煤气(混合气体,其微观示意图如图所示( )
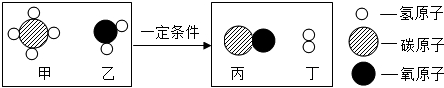
根据以上微观示意图得到的结论中,正确的是( )

根据以上微观示意图得到的结论中,正确的是( )
| A. | 该反应是置换反应 | B. | 反应中氢元素有化合态变为游离态 | ||
| C. | 反应前后,分子、原子的种类均不变 | D. | 反应中丙丁分子数比为1:1 |
7.下列有关实验现象的描述,正确的是( )
| A. | 镁条在空气中燃烧发出蓝紫色火焰,产生大量白烟 | |
| B. | 电解水正极一侧得到的气体能使带火星的木条复燃 | |
| C. | 细铁丝在氧气中燃烧,火星四射,生成红棕色固体 | |
| D. | 打开浓硫酸的试剂瓶盖时,瓶口有白雾产生 |
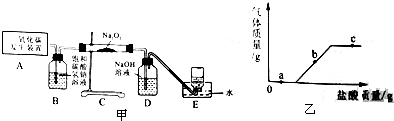

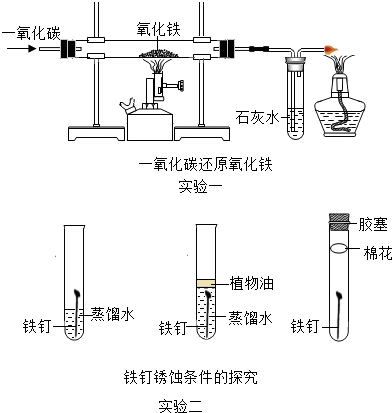 初中化学教材中的一些实验如图所示,请你回答下列问题:
初中化学教材中的一些实验如图所示,请你回答下列问题: