题目内容
4.某三价金属氧化物中氧元素质量分数为30%,则该金属的相对原子质量为56.分析 先依据金属元素和氧元素的化合价写出该金属氧化物的化学式,再设该金属的相对原子质量为x,最后根据氧元素的质量分数为30%,即可算出该金属的相对原子质量.
解答 解:设该金属元素为R,因为该金属元素在其氧化物中显示+3价,则其氧化物的化学式为:R2O3;
设R的相对原子质量为x,则$\frac{16×3}{2x+16×3}$×100%=30%,解得x=56;
故答案为:56.
点评 主要考查了元素质量分数的计算方法;某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{该物质的相对分子质量}$×100%.

练习册系列答案
相关题目
11.下列除杂设计正确的是( )
| 序号 | 物 质 | 杂 质 | 所用试剂或方法 |
| A | CO2 | CO | 点燃 |
| B | CaCl2溶液 | 盐酸 | 过量CaCO3,过滤 |
| C | Fe | Cu | 加入过量的稀硫酸,过滤,洗涤,干燥 |
| D | MnO2 | KCl | 溶解,过滤,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
19.元素S的相对原子质量为32,它的氧化物含氧60%,则该氧化物的化学式为( )
| A. | SO2 | B. | SO | C. | SO3 | D. | S2O3 |
14.医师建议多吃蔬菜、水果.从你所学知识判断,补充的营养素是( )
| A. | 糖类 | B. | 维生素 | C. | 油脂 | D. | 蛋白质 |
 钙的常见化合价是:+2,CaSO4中硫元素化合价+6.
钙的常见化合价是:+2,CaSO4中硫元素化合价+6.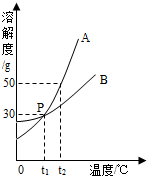 如图是A、B两种物质的溶解度曲线.据图回答:
如图是A、B两种物质的溶解度曲线.据图回答: ,由此可写出各步反应的化学方程式.硫及硫的化合物间的转化关系可表示为:
,由此可写出各步反应的化学方程式.硫及硫的化合物间的转化关系可表示为: .
.