题目内容
4.下列关于Fe、Fe2+的说法中,正确的是( )| A. | 它们的核外电子数相同 | B. | 它们的质子数相同 | ||
| C. | 它们的最外层电子数相同 | D. | 它们的性质完全相同 |
分析 根据Fe、Fe2+两种微粒可知,它们是用同种元素的不同微粒,具有相同的质子数和不同的电子数
解答 解:A、因金属原子失去电子变为金属阳离子,且Fe2+、Fe带电荷不同,则原子与该离子的电子数一定不同,故A错;
B、它们是同种元素形成的微粒,原子核的结构相同,但核外电子数不同,则它们的质子数相同,故B正确;
C、因金属原子失去电子变为金属阳离子,且Fe2+、Fe带电荷的情况不同,则原子与该离子的电子数一定不同,所以最外层电子数也一定不同,故C错;
D、因Fe、Fe2+两种粒子的核外电子数不同,所以其最外层电子数也不同,而最外层电子数决定了元素的化学性质,所以两者化学性质一定不同,故D错.
故选:B.
点评 本题考查同种元素形成的微粒的关系和性质,学生应明确它们的区别和联系,把握化学式的不同,意义不同性质不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.判断镁带燃烧是化学变化的主要依据( )
| A. | 发出耀眼的白光 | B. | 生成白色固体 | C. | 放出大量的热 | D. | 燃烧后质量增加 |
15.当前在非洲蔓延的埃博拉病毒备受世人关注,帕拉米韦是治疗病毒的一种新药,其化学式是C15H28N4O4,有关帕拉米韦的说法错误的是( )
| A. | 它的一个分子中含有51个原子 | |
| B. | 它是由碳、氢、氮、氧四种元素组成 | |
| C. | 其分子中碳、氢、氧原子个数比为15:28:4 | |
| D. | 其中的氢元素质量分数最高 |
19.图1是部分实验室制取气体的装置图:

(1)写出图中标有①、②的仪器名称试管、集气瓶
(2)老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.请你根据所学知识进行探究:
①此气体是什么物质?验证它的实验方案如下:
②若用此方法制取该气体,发生装置将选取图2中的A或B(填序号,以下同),收集装置选取D或E.
③如果用如图所示装置收集所猜想的气体,你认为气体应从a端(填“a”或“b”)导入.

(1)写出图中标有①、②的仪器名称试管、集气瓶
(2)老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.请你根据所学知识进行探究:
①此气体是什么物质?验证它的实验方案如下:
| 猜 想 | 验证猜想的实验步骤 | 现象及结论 |
| 我认为此气体可能是氧气 | ||
产生此气体的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | ||
③如果用如图所示装置收集所猜想的气体,你认为气体应从a端(填“a”或“b”)导入.
9.如图所示操作中正确的是( )
| A. | 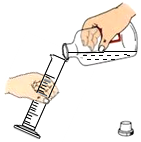 向量筒中倾倒溶液 | B. |  加热试管中的液体 | ||
| C. | 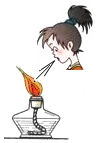 熄灭酒精灯 | D. | 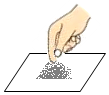 取用粉末状药品 |