题目内容
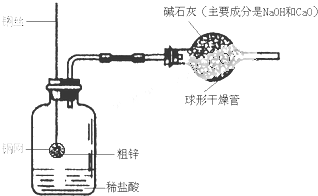 某同学设计了一套如下图所示的装置,并用该装置测定粗锌样品的含锌量.
某同学设计了一套如下图所示的装置,并用该装置测定粗锌样品的含锌量.(1)称量10.0g粗锌放在铜网中,按图将仪器组装好以后,称得仪器和药品总质量为120.0g.
(2)将铜网插入足量稀盐酸中,充分反应,可以观察到的实验现象为
产生气泡
产生气泡
,反应的化学方程式为Zn+2HCl=ZnCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
.(3)反应完全后,称得装置总质量为119.8g.则粗锌的纯度为
65%
65%
.(4)该实验中碱石灰的作用是干燥剂,同时防止稀盐酸挥发出的氯化氢气体逸散到空气中.若不用碱石灰,则所测定的粗锌纯度
偏大
偏大
(填“偏大”、“偏小”或“无影响”;(5)若将粗锌换成石灰石,原实验方案
不能
不能
(填“能”或“不能”)用于石灰石样品纯度的测定,理由是碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量
碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量
.分析:(2)根据锌与盐酸反应生成氯化锌和氢气,产生气泡进行解答;
(3)根据氢气的质量=120g-119.8g=0.2g,根据化学方程式列比例式求得锌的质量进行解答;
(4)根据稀盐酸挥发出的氯化氢气体逸散到空气中,使装置总质量减小,氢气的质量偏大求得锌的质量也偏大,所测定的粗锌纯度偏大进行解答;
(5)根据碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量进行解答.
(3)根据氢气的质量=120g-119.8g=0.2g,根据化学方程式列比例式求得锌的质量进行解答;
(4)根据稀盐酸挥发出的氯化氢气体逸散到空气中,使装置总质量减小,氢气的质量偏大求得锌的质量也偏大,所测定的粗锌纯度偏大进行解答;
(5)根据碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量进行解答.
解答:解:(2)锌与盐酸反应生成氯化锌和氢气,产生气泡,反应的化学方程式为 Zn+2HCl=ZnCl2+H2↑;
(3)设参加反应锌的质量为x.氢气的质量=120g-119.8g=0.2g,
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.2g
=
x=0.2g
粗锌的纯度=
×100%=65%
答:粗锌的纯度为65%.
(4)稀盐酸挥发出的氯化氢气体逸散到空气中,使装置总质量减小,氢气的质量偏大求得锌的质量也偏大,所测定的粗锌纯度偏大;
(5)碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量.
故答案为:(2)产生气泡;Zn+2HCl=ZnCl2+H2↑;
(3)65%;
(4)偏大;
(5)不能; 碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量.
(3)设参加反应锌的质量为x.氢气的质量=120g-119.8g=0.2g,
Zn+2HCl=ZnCl2+H2↑
65 2
x 0.2g
| 65 |
| x |
| 2 |
| 0.2g |
x=0.2g
粗锌的纯度=
| 6.5g |
| 10g |
答:粗锌的纯度为65%.
(4)稀盐酸挥发出的氯化氢气体逸散到空气中,使装置总质量减小,氢气的质量偏大求得锌的质量也偏大,所测定的粗锌纯度偏大;
(5)碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量.
故答案为:(2)产生气泡;Zn+2HCl=ZnCl2+H2↑;
(3)65%;
(4)偏大;
(5)不能; 碱石灰能吸收二氧化碳和水蒸气等气体,导致不能测出CO2的质量.
点评:本题考查了图示和化学反应相结合的通过化学方程式进行计算,问题难度逐渐加大;解答本题的关键是能够从字意中找出数量关系,掌握反应的情况;对学生理解的能力要求较高.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目




