题目内容
(1)镁元素的原子序数为 ,元素符号为 .
(2)镁原子的结构示意图为 (填字母).
A、 B、
B、
(3)镁元素与氯元素形成的化合物的化学式为 .
(4)下列对原子构成的理解错误的是 (填字母).
A.原子整体不显电性 B.原子核比原子小得多
C.原子核是不可分割的实心球体 D.原子质量主要集中在原子核上.
(2)镁原子的结构示意图为
A、
 B、
B、
(3)镁元素与氯元素形成的化合物的化学式为
(4)下列对原子构成的理解错误的是
A.原子整体不显电性 B.原子核比原子小得多
C.原子核是不可分割的实心球体 D.原子质量主要集中在原子核上.
考点:元素周期表的特点及其应用,原子的定义与构成,原子结构示意图与离子结构示意图,化学式的书写及意义
专题:物质的微观构成与物质的宏观组成,化学用语和质量守恒定律
分析:(1)根据镁元素的原子序数和元素符号来解答;(2)在原子中,核电荷数=质子数=核外电子数;(3)根据两元素的化合价来书写化合物的化学式;(4)熟知原子的构成,原子由带电的原子核和核外电子构成,原子核又是由带电的质子和不带电的中子构成,原子的质量主要集中在原子核上.即,原子的质量≈原子核的质量=质子质量+中子质量.
解答:解:(1)镁是12号元素,原子序数为12,其元素符号为:Mg;
(2)在原子中,核电荷数=质子数=核外电子数,A中质子数=核外电子数,属于镁原子;B中质子数>核外电子数,属于镁离子;
(3)在化合物中,镁元素显+2价,氯元素显-1价,故氯化镁的化学式为:MgCl2;
(4)A、原子中的质子数等于核电荷数还等于核外电子数,所带正负电荷总数相等,所以原子整体不显电性,故A说法正确;
B、原子核的体积很小,比原子小得多,故B说法正确;
C、原子可以分为原子核和核外电子,并且原子内部有很大的空间,故C说法错误;
D、原子核的体积很小,但质量很大,原子的质量主要集中在原子核上,核外电子的质量很小可以忽略不计,故D说法正确.
故答案为:(1)12;Mg;(2)A;(3)MgCl2;(4)C.
(2)在原子中,核电荷数=质子数=核外电子数,A中质子数=核外电子数,属于镁原子;B中质子数>核外电子数,属于镁离子;
(3)在化合物中,镁元素显+2价,氯元素显-1价,故氯化镁的化学式为:MgCl2;
(4)A、原子中的质子数等于核电荷数还等于核外电子数,所带正负电荷总数相等,所以原子整体不显电性,故A说法正确;
B、原子核的体积很小,比原子小得多,故B说法正确;
C、原子可以分为原子核和核外电子,并且原子内部有很大的空间,故C说法错误;
D、原子核的体积很小,但质量很大,原子的质量主要集中在原子核上,核外电子的质量很小可以忽略不计,故D说法正确.
故答案为:(1)12;Mg;(2)A;(3)MgCl2;(4)C.
点评:本题考查原子构成,注重基础,学习中应注意对原子构成的理解和一些规律知识的掌握和运用.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
下列物质的化学式中,书写错误的是( )
| A、碳酸钠 NaCO3 |
| B、氧化钙 CaO |
| C、硝酸钙 Ca(NO3)2 |
| D、硫酸锌 ZnSO4 |
通过下列实验可以得出的结论,其中不合理的是:( )


| A、甲实验中说明水是由氢、氧两种元素组成的 |
| B、乙实验既可以说明分子在不停的运动着,又可以说明氨水显碱性 |
| C、丙实验既可以说明二氧化碳能溶于水,又可以说明二氧化碳具有酸性 |
| D、丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
钠原子的结构示意图为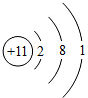 ,下列关于它的说法错误的是( )
,下列关于它的说法错误的是( )
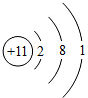 ,下列关于它的说法错误的是( )
,下列关于它的说法错误的是( )| A、钠原子的核电荷数为11 |
| B、钠原子核外共有3层电子 |
| C、钠原子易失去最外层电子 |
| D、钠原子和钠离子的化学性质相同 |
下列微粒的结构示意图中,表示阴离子的是( )
A、 |
B、 |
C、 |
D、 |
