题目内容
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,某研究小组在实验室里以废铜屑为原料制取碱式碳酸铜,若实验得到2.42g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80g固体,此样品中碱式碳酸铜的质量分数是多少?
【答案】分析:此题是典型的量差反计算题,根据反应前后固体质量的变化利用方程式的有关计算解决即可;
解答:解:设此样品中碱式碳酸铜的质量为x
Cu2(OH)2CO3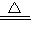 2CuO+H2O+CO2↑△m(减小量)
2CuO+H2O+CO2↑△m(减小量)
222 160 222-160=62
x (2.42g-1.8g)=0.62g
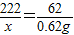
x=2.22g
此样品中碱式碳酸铜的质量分数是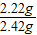 ×100%=91.7%
×100%=91.7%
答:此样品中碱式碳酸铜的质量分数是91.7%;
点评:此题是根据化学方程式计算的基础题,解题的关键是找到固体质量之差的含义和应用;
解答:解:设此样品中碱式碳酸铜的质量为x
Cu2(OH)2CO3
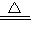 2CuO+H2O+CO2↑△m(减小量)
2CuO+H2O+CO2↑△m(减小量)222 160 222-160=62
x (2.42g-1.8g)=0.62g
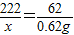
x=2.22g
此样品中碱式碳酸铜的质量分数是
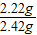 ×100%=91.7%
×100%=91.7%答:此样品中碱式碳酸铜的质量分数是91.7%;
点评:此题是根据化学方程式计算的基础题,解题的关键是找到固体质量之差的含义和应用;

练习册系列答案
相关题目



