题目内容
14.实验室常用下列装置制取气体,请你根据所学知识回答下列问题.
(1)写出所指仪器的名称:a长颈漏斗.
(2)如图所示的装置图中有明显错误的是A、D(填序号).
(3)实验室选用B和E装置制取氧气的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)实验室用高锰酸钾制取氧气并用排水法收集的操作,下列叙述正确的是ABC.
A.先检查装置的气密性,再加入药品进行制取
B.先均匀预热,再对着药品部位集中加热
C.先等着导管口排出的气泡连续均匀后,再将导管伸入盛水的集气瓶中进行收集
D.先熄灭酒精灯,再将导管从水槽中取出.
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.如图所示的装置图中有明显错误的是A,试管口应该略向下倾斜;D中导管应该伸入集气瓶的底部;实验室用高锰酸钾制取氧气并用排水法收集的操作,叙述正确的是:先检查装置的气密性,再加入药品进行制取;先均匀预热,再对着药品部位集中加热;先等着导管口排出的气泡连续均匀后,再将导管伸入盛水的集气瓶中进行收集;先熄灭酒精灯,再将导管从水槽中取出不正确,会造成水倒流而炸裂试管.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)如图所示的装置图中有明显错误的是A,试管口应该略向下倾斜;D中导管应该伸入集气瓶的底部;故答案为:A、D;
(3)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)实验室用高锰酸钾制取氧气并用排水法收集的操作,叙述正确的是:先检查装置的气密性,再加入药品进行制取;先均匀预热,再对着药品部位集中加热;先等着导管口排出的气泡连续均匀后,再将导管伸入盛水的集气瓶中进行收集;先熄灭酒精灯,再将导管从水槽中取出不正确,会造成水倒流而炸裂试管;故答案为:ABC;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案| A. | 若生成物C和D分别为盐和水,则反应物一定是酸和碱 | |
| B. | 若A、C是单质,B、D是化合物,则该反应类型一定是置换反应 | |
| C. | 若A、B、C、D均为化合物,则该反应一定是复分解反应 | |
| D. | 若A、B各取10克使其充分反应,则生成C、D的质量总和一定等于20克 |
| A. | 反应物都属于氧化物 | |
| B. | 该反应使有害气体转化为无害物质 | |
| C. | 反应前后元素的种类、原子和分子个数都不变 | |
| D. | 化学反应方程式中所表示的反应物和生成物中只有一种物质是单质 |
| A. | 碱的溶液呈碱性,则碱性液体一定是碱的溶液 | |
| B. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| C. | 单质中只含有一种元素,则只含有一种元素的纯净物一定是单质 | |
| D. | 碳酸盐与盐酸反应生成气体,则与盐酸反应生成气体的物质一定是碳酸盐 |
【资料卡片】(1)碳酸钠(Na2CO3),俗名苏打、纯碱,具有热稳定性,易溶于水,其水溶液呈碱性.
(2)碳酸氢钠(NaHCO3),俗称“小苏打”.固体50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,270℃时完全分解.水溶液呈现弱碱性.
实验一、实验装置如图Ⅰ~Ⅳ所示.

(1)若用碳酸钠制取二氧化碳气体并验证二氧化碳的部分化学性质,应选用实验Ⅰ,验证二氧化碳化学性质的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(2)实验Ⅱ说明泡沫灭火器中选择碳酸氢钠与酸反应制CO2而不选择碳酸钠.
(3)若用实验Ⅳ来验证碳酸钠的热稳定性大于碳酸氢钠,则试管B中装入的固体最好是NaHCO3,能说明碳酸钠比碳酸氢钠稳定的实验现象是左边试管中澄清石灰水变浑浊,右边试管中澄清石灰水不变浑浊.
(4)实验Ⅲ可用于测定Na2CO3固体中混有的少量NaHCO3的质量分数,需测定的数据有固体样品的质量和沉淀总质量(或反应前后固体的质量).
实验二、用碳酸钠溶液与石灰水反应制烧碱.
取一定量的碳酸钠溶液与澄清石灰水充分反应,过滤,通过实验探究滤液中溶质成分.
【提出问题】滤液中含有哪些溶质?
【原理分析】碳酸钠与石灰水反应的原理为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH(用化学方程式表示).
【提出假设】假设一:滤液中只含氢氧化钠;
假设二:滤液中含氢氧化钠和氢氧化钙;
假设三:滤液中含氢氧化钠和碳酸钠.
【实验方案】
| 实验步骤 | 实验现象 | 实验结论 |
| 甲同学取少量滤液于试管中, 再滴入氯化钙溶液 | 若产生沉淀 | 碳酸钠过量 |
| 若无明显现象 | 恰好反应 |
| 实验步骤 | 现象和结论 |
| 取少量滤液于试管中,滴入②碳酸钠溶液 | 观察到③无明显变化,说明恰好反应 |
| A. | 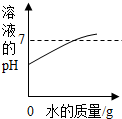 向一定量稀硫酸中滴加水 | |
| B. |  向一定量纯碱和烧碱的混合溶液中滴入盐酸 | |
| C. | 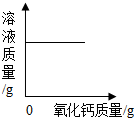 一定温度时向一定量饱和石灰水中加入氧化钙 | |
| D. | 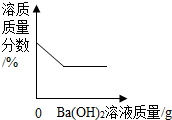 向稀硫酸中慢慢滴加Ba(OH)2溶液至过量 |
| A. | 钢铁门窗比铝合金门窗更耐腐蚀 | |
| B. | 化肥KN03比NH4NO3营养元素种类多 | |
| C. | 青少年缺钙会患佝偻病和发育不良 | |
| D. | 种植吃叶的蔬菜,应施用较多的氮肥 |
| 序号 | 物质 | 杂质 | 所用试剂和操作方法 |
| A | CO2 | HCl | 将混合气体通过AgNO3溶液 |
| B | NaNO3溶液 | Na2SO4 | 加入过量的Ba(NO3)2溶液,过滤 |
| C | NaOH溶液 | Na2CO3 | 加入适量CaCl2溶液、过滤 |
| D | 铁粉 | Fe2O3 | 加入适量的稀盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
 应用所学知识,回答下列有关金属的问题:
应用所学知识,回答下列有关金属的问题: