题目内容
高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
(1)试管尾部放一团湿棉花的目的是 。
(2)探究生成的气体是什么? 用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是______________。写出该反应的化学方程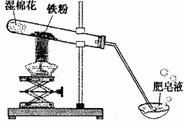 式 。
式 。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 与盐酸反应 | FeCl2+H2O | FeCl3+H2O | FeCl2+ FeCl3+H2O |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是 ;猜想二:剩余固体________。
【实验探究】(每空2分)
| 实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为_______________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
(4)若反应前称得铁的质量为2.1g,高温下,铁与水反应结束称得固体质量为2.8 g则剩余固体成分是 。(通过计算说明,要求写出计算过程)
g则剩余固体成分是 。(通过计算说明,要求写出计算过程)
答案 (1)提供水蒸气;
(2)H2; 2H2+O2 2H2O
2H2O
(3)【猜想与假设】猜想一:Fe 、Fe3O 4 猜想二Fe3O4
4 猜想二Fe3O4
【实验探究】
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体 | 若固体全部溶解,没有气泡冒出,剩余固体是Fe3O4. 若固体全部溶解,有气泡冒出,剩余固体是Fe与Fe3O4. |
【实验结论】3Fe+4H2O高温Fe3O4+4H2↑;
【反思与交流】Fe2O3红棕色粉末
(4)固体成分是Fe 、Fe3O4

 阅读快车系列答案
阅读快车系列答案暖宝宝是一种防寒用品,如图所示.暖宝宝中的主要成分有哪些?发热的原因是什么?
(1)小明探究:暖宝宝中的主要成分是什么?剪开内包装袋,倒出其中的粉末,发现呈黑色.
【提出猜想】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化
三铁中的一种或几种.
【初步验证】将磁铁靠近黑色粉末,部分被吸引.
【查阅资料】四氧化三铁具有磁性,能被磁铁吸引.
【得出结论】该黑色粉末可能含有 .
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取黑色粉末加足量稀硫酸 | 固体部分溶解,有气泡产生,溶液无蓝色 |
| ② | 取实验①的残渣灼烧,将内壁涂有 澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
由实验①可知,该黑色粉末肯定含 ,肯定不含 .写出实验①的化学反应方程式 .
由实验②可知,该黑色粉末肯定含 .
(2)小明思考:暖宝宝为什么会发热?
【查阅资料】暖宝宝中的铁粉在空气中发生了缓慢氧化,进而放出热量.由此可见,人们可以利用化学反应放出的能量,请再举一例: .
(3)人们利用化学反应还可以 .

金属是一种重要的材料,人类的生活和生产都离不开金属,全世界每年因生锈损失的钢铁,约占世界年产量的十分之一.
(1)兴趣小组的同学想探究钢铁锈蚀的条件,他将一个干净的铁钉放入试管中(如图一),定期观察并记录现象.图一中最先锈蚀的部位 (填写A、B或C);举出一种防止钢铁锈蚀的具体方法 ;

(2)根据图二的应用实例,试说出金属具有的一点物理性质 ;
(3)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,原因是 ;
(4)下表中不同的金属被开发、利用的年代不同,决定这一先后顺序的关键因素是 ;

A.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量
(5)用质量相等的镁粉和铝粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如图三所示.则下列说法中正确的是 ;
A.曲线a、b分别表示镁、铝的反应情况
B.盐酸均反应完,镁恰好完全反应,铝剩余
C.盐酸均反应完,镁、铝也恰好完全反应
D.镁、铝都反应完,盐酸有剩余

(6)联想到工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图四所示
①A、B处发生的现象分别是A 、B ;
②为了防止溶液倒吸,本实验停止加热前是否要先断开A和B的连接处? (填“需要”或“不需要”),理由是 气体会一直通到装置冷却,不会发生倒吸 .
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品的质量/g | 166.5 | 166.3 | 166.1 | 166.1 |
(7)兴趣小组的同学又准确称取了11.5克生铁样品,放入装有100.0g稀硫酸(足量)的烧杯中(烧杯质量为55.0g).在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,
记录如表.求:①反应中产生氢气 克;②反应后所得溶液中溶质质量分数.(结果精确到0.1%)

 质可能为____________(只写一种);
质可能为____________(只写一种); 因煤气泄漏出现较大气味时,应立即关闭气阀,不能打开抽油烟机排气
因煤气泄漏出现较大气味时,应立即关闭气阀,不能打开抽油烟机排气