题目内容
6.一定条件下24gCH4和一定量的氧气恰好完全反应,生成54gH2O、22gCO2和28gX,下列说法不正确的是( )| A. | 参加反应的氧气的质量为80g | |
| B. | 反应的化学方程式中CO2和H2O的化学计量数之比为2:1 | |
| C. | 若增加16gO2,甲烷能完全燃烧生成CO2和H2O | |
| D. | X的化学式为CO |
分析 根据质量守恒定律计算参加反应的氧气的质量;根据 CO2和 H2O 的质量计算化学计量数之比;根据,24g CH4完全燃烧所需氧气的量计算.
解答 解:A、根据质量守恒定律,参加反应的氧气的质量为:54g+22g+28g-24g=80g;故正确;
B、化学方程式中 CO2和 H2O 的化学计量数之比为:$\frac{22g}{44}:\frac{54g}{18}$=1:6;故错误;
C、设24g CH4完全燃烧所需氧气的质量为x
CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
16 64
24g x
$\frac{16}{24g}=\frac{64}{x}$
x=96g
故需增加氧气的质量为:96g-80g=16g,故正确;
D、一定条件下,24gCH4与80gO2恰好完全反应,生成54gH2O、22gCO2和28gX,24gCH4中含有碳元素的质量为:24g×$\frac{12}{16}$=18g,故含有氢元素的质量为:24g-18g=6g;54gH2O中含有氢元素的质量为:54g×$\frac{2}{18}$×100%=6g;22gCO2中含有碳元素的质量为:22g×$\frac{12}{44}$=6g,故X中含有18g-6g=12g的碳,不含有氢元素,含有氧元素的质量为:80g-(54g-6g)-(22g-6g)=16g,故X中碳原子和氧原子的原子个数比为:$\frac{12g}{12}:\frac{16g}{16}$=1:1.故该物质是一氧化碳,故正确;
故选:B.
点评 本题考查学生质量守恒定律的应用以及利用化学反应方程式的计算,并注意计算格式的规范.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
17.下列有关金属的说法正确的是( )
| A. | 生铁是化合物 | B. | 合金一定不含非金属 | ||
| C. | 铝有良好的抗氧化能力 | D. | 赤铁矿是金属材料 |
14.被媒体爆光的“奶粉事件”中,造假分子向奶粉中添加了三聚氰胺,三聚氰胺形状为纯白色单斜棱晶体,分子式C3N6H6,下列有关它的说法正确的是( )
| A. | 三聚氰胺是由15个原子构成 | |
| B. | 三聚氰胺是一种氧化物 | |
| C. | 三聚氰胺的相对分子质量是126 | |
| D. | 三聚氰胺中碳、氮、氢元素的质量比为1:2:2 |
1.下列关于燃烧现象的描述,正确的是( )
| A. | 红磷在空气中燃烧产生大量的白雾 | |
| B. | 硫在空气中燃烧发出蓝紫色火焰 | |
| C. | 镁条在氧气中燃烧发出耀眼的白光、生成黑色固体 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射 |
11.如图为初中化学常见气体的发生与收集装置.有关这些装置,下列说法中不正确的是( )


| A. | 装置Ⅱ、Ⅳ组合可制取氧气 | |
| B. | 装置Ⅰ可作为固体加热制取气体的发生装置 | |
| C. | 装置Ⅱ中长颈漏斗可以用分液漏斗、医用注射器代替 | |
| D. | 装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应的气体 |
4.如图漫画中,发生化学变化的步骤是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
2.下列各组元素的原子结构示意图中具有相似化学性质的元素是( )
| A. | 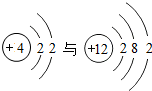 | B. | 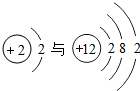 | ||
| C. | 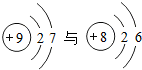 | D. | 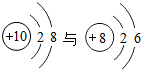 |
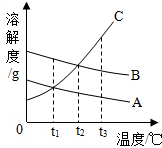 如图是A、B、C三种固体物质的溶解度曲线,试看图后回答:
如图是A、B、C三种固体物质的溶解度曲线,试看图后回答: