题目内容
已知化肥硝酸铵的化学式为NH4NO3,计算:
(1)硝酸铵中氮元素的质量分数为 ;
(2)多少克硝酸铵中含氮元素140g.
(1)硝酸铵中氮元素的质量分数为
(2)多少克硝酸铵中含氮元素140g.
考点:元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)利用化合物的质量等于元素的质量除以该元素的质量分数进行分析解答.
| 相对原子质量×原子个数 |
| 相对分子质量 |
(2)利用化合物的质量等于元素的质量除以该元素的质量分数进行分析解答.
解答:解:(1)NH4NO3中氮元素的质量分数为
×100%=35%.
(2)含N元素为140g的硝酸铵的质量为140g÷35%=400g.
答:(1)35%;(2)400g
| 14×2 |
| 14×2+1×4+16×3 |
(2)含N元素为140g的硝酸铵的质量为140g÷35%=400g.
答:(1)35%;(2)400g
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
下列四种粒子的结构示意图中,属于阳离子的是( )
A、 |
B、 |
C、 |
D、 |
如图所示的实验操作中,正确的是( )
A、 |
B、 |
C、 |
D、 |
金属M与AgNO3溶液反应的化学方程式为:M+2AgNO3═M(NO3)2+2Ag.则下列说法错误的是( )
| A、金属M不可能是铝 |
| B、M的金属活动性比Ag强 |
| C、该反应属于分解反应 |
| D、该反应前后M的化合价发生了改变 |
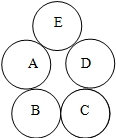 A、B、C、D、E分别是氧化铁、铁、氧气、单质碳、稀硫酸中的一种物质,用五个圆表示这五种物质,用两圆相切表示两种物质可以发生化学反应,请回答下列问题:
A、B、C、D、E分别是氧化铁、铁、氧气、单质碳、稀硫酸中的一种物质,用五个圆表示这五种物质,用两圆相切表示两种物质可以发生化学反应,请回答下列问题: