题目内容
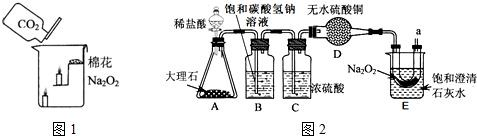
化学兴趣小组的同学根据启普发生器原理,设计了如图装置制备二氧化碳,并进行某些性质实验.先将大理石放在隔板上,反应时,盐酸从长颈漏斗中加入.(1)写出反应的化学方程式______.
(2)简述如何证明集气瓶里的二氧化碳已充满______.
(3)若向上述集气瓶里倒入澄清石灰水,发生反应的化学方程式是:______.
(4)实验室制氢气用的稀盐酸的溶质质量分数为10%,如需37克此浓度的稀盐酸,则需37%的浓盐酸与水按______的质量比配制而成.

【答案】分析:(1)大理石的主要成分为碳酸钙,和盐酸反应生成二氧化碳、水和氯化钙,可以据此写出化学方程式,注意配平;
(2)二氧化碳不能燃烧也不支持燃烧,可以据此选择验满的方法;
(3)澄清石灰水的主要成分为氢氧化钙,可以和二氧化碳反应,可以据此来完成该题的解答;
(4)根据溶液稀释前后溶液中溶质的质量不变来完成解答.
解答:解:(1)大理石的主要成分为碳酸钙,和盐酸反应生成二氧化碳、水和氯化钙,该化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)二氧化碳不能燃烧也不支持燃烧,所以可以将燃着的木条放在集气瓶口,如果木条熄灭则说明收集满了,反之不满;
(3)澄清石灰水的主要成分为氢氧化钙,可以和二氧化碳反应,产生白色的碳酸钙沉淀,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(4)设需水的质量为x,则需37%的盐酸的质量为(37g-x),根据稀释前后溶液中溶质的质量不变可以知道:
37g×10%=(37g-x)×37%
解得:x=27g
所以需37%的浓盐酸与水的质量比为:(37g-27g):27g=10:27;
答:需37%的浓盐酸与水的质量比为10:27.
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)将燃着的木条放在集气瓶口,如果木条熄灭则说明收集满了;
(3)Ca(OH)2+CO2═CaCO3↓+H2O;
(4)10:27.
点评:熟练掌握二氧化碳的制取、检验和验满的方法,并能写出相关的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;Ca(OH)2+CO2═CaCO3↓+H2O.
(2)二氧化碳不能燃烧也不支持燃烧,可以据此选择验满的方法;
(3)澄清石灰水的主要成分为氢氧化钙,可以和二氧化碳反应,可以据此来完成该题的解答;
(4)根据溶液稀释前后溶液中溶质的质量不变来完成解答.
解答:解:(1)大理石的主要成分为碳酸钙,和盐酸反应生成二氧化碳、水和氯化钙,该化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)二氧化碳不能燃烧也不支持燃烧,所以可以将燃着的木条放在集气瓶口,如果木条熄灭则说明收集满了,反之不满;
(3)澄清石灰水的主要成分为氢氧化钙,可以和二氧化碳反应,产生白色的碳酸钙沉淀,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(4)设需水的质量为x,则需37%的盐酸的质量为(37g-x),根据稀释前后溶液中溶质的质量不变可以知道:
37g×10%=(37g-x)×37%
解得:x=27g
所以需37%的浓盐酸与水的质量比为:(37g-27g):27g=10:27;
答:需37%的浓盐酸与水的质量比为10:27.
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)将燃着的木条放在集气瓶口,如果木条熄灭则说明收集满了;
(3)Ca(OH)2+CO2═CaCO3↓+H2O;
(4)10:27.
点评:熟练掌握二氧化碳的制取、检验和验满的方法,并能写出相关的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;Ca(OH)2+CO2═CaCO3↓+H2O.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.
20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.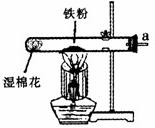 37、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.
37、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究. 21、某化学兴趣小组的同学在对氧气性质进行研究时,设计了如下实验:
21、某化学兴趣小组的同学在对氧气性质进行研究时,设计了如下实验:
 横店中学化学兴趣小组的同学在做铁和硫酸铜溶液反应的实验时意外发现铁丝的表面有少量的、无色无味的气体产生,他们对该现象产生了浓厚的兴趣,想探究一下该气体的成分.
横店中学化学兴趣小组的同学在做铁和硫酸铜溶液反应的实验时意外发现铁丝的表面有少量的、无色无味的气体产生,他们对该现象产生了浓厚的兴趣,想探究一下该气体的成分.