题目内容
将一根锃亮的铁丝放入蓝色的硫酸铜溶液中,过一会儿,发现铁丝表面出现了红色物质.
(1)写出发生反应的化学方程式 .
(2)反应后所得溶液质量比反应前 (填“增加”、“减少”).
(3)在化学反应中,元素化合价升高的反应物是还原剂,元素化合价降低的反应物是氧化剂.试判断上述反应中,氧化剂是 .铁的化学性质比较活泼,在纯氧中燃烧的现象是 ,化学方程式为 .铁在潮湿的空气中易生锈,铁锈的主要成分是 ;铁锈很 ,不能阻碍里层的铁继续与氧气、水蒸气等反应,因此,铁制品表面的锈如不及时除去,会加快铁制品的生锈速度.
(1)写出发生反应的化学方程式
(2)反应后所得溶液质量比反应前
(3)在化学反应中,元素化合价升高的反应物是还原剂,元素化合价降低的反应物是氧化剂.试判断上述反应中,氧化剂是
考点:金属的化学性质,金属锈蚀的条件及其防护,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:在金属活动性顺序中,只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,根据这一规律可以判断反应的发生及验证金属的活动性强弱.
铁在氧气中燃烧很剧烈,火星四射,放出大量的热,生成黑色固体.铁和氧气反应生成四氧化三铁,铁锈是一种疏松多孔的物质,铁锈的主要成分可以用Fe2O3来表示.
铁在氧气中燃烧很剧烈,火星四射,放出大量的热,生成黑色固体.铁和氧气反应生成四氧化三铁,铁锈是一种疏松多孔的物质,铁锈的主要成分可以用Fe2O3来表示.
解答:解:
(1)由于在金属活动性顺序中,铁在铜前,因此铁可以和硫酸铜溶液反应生成铜和硫酸亚铁,故化学方程式为:Fe+CuSO4═FeSO4+Cu
(2)由于铁可以和硫酸铜溶液反应,56份质量的铁与硫酸铜溶液反应,生成64份质量的铜,故反应后所得溶液质量比反应前减少.
(3)由于铁元素的化合价有0→+2,而铜元素由+2→0,因此硫酸铜是氧化剂,故答案为:CuSO4.
铁在纯氧中燃烧的现象是:剧烈燃烧,火星四射,放出大量的热,生成黑色固体.铁在氧气中燃烧的化学方程式为:3Fe+2O2
Fe3O4.铁锈的主要成分是Fe2O3.铁锈是一种疏松多孔的物质,如不及时除去,会加快铁制品的生锈速度.
故答案为:
(1)Fe+CuSO4═FeSO4+Cu.
(2)减少.
(3)CuSO4. 剧烈燃烧,火星四射,放出大量的热,生成黑色固体,3Fe+2O2
Fe3O4. Fe2O3; 疏松多孔
(1)由于在金属活动性顺序中,铁在铜前,因此铁可以和硫酸铜溶液反应生成铜和硫酸亚铁,故化学方程式为:Fe+CuSO4═FeSO4+Cu
(2)由于铁可以和硫酸铜溶液反应,56份质量的铁与硫酸铜溶液反应,生成64份质量的铜,故反应后所得溶液质量比反应前减少.
(3)由于铁元素的化合价有0→+2,而铜元素由+2→0,因此硫酸铜是氧化剂,故答案为:CuSO4.
铁在纯氧中燃烧的现象是:剧烈燃烧,火星四射,放出大量的热,生成黑色固体.铁在氧气中燃烧的化学方程式为:3Fe+2O2
| ||
故答案为:
(1)Fe+CuSO4═FeSO4+Cu.
(2)减少.
(3)CuSO4. 剧烈燃烧,火星四射,放出大量的热,生成黑色固体,3Fe+2O2
| ||
点评:本题难度不大,主要考查了对金属活动性顺序的应用,从而培养学生对金属活动性顺序的理解和应用.

练习册系列答案
相关题目
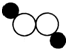 如图是某物质分子结构模拟图.图中“○”表示氧原子.“●”表示氢原子.请根据图示回答:
如图是某物质分子结构模拟图.图中“○”表示氧原子.“●”表示氢原子.请根据图示回答: