题目内容
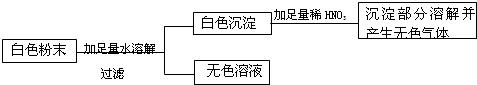
有一包白色粉末,可能由CaCO3、NaCl、CuSO4、Na2SO4和Ba(NO3)2中的一种或几种组成.为确定其组成,小明同学进行了如下探究活动:
步骤①:取少量白色粉末,加足量水充分溶解后过滤,得到白色沉淀和无色滤液.
步骤②:取步骤①得到的白色沉淀,加入足量稀硝酸,沉淀部分溶解,并有无色气体产生,将气体通入澄清的石灰水中,石灰水变浑浊.
通过分析可知:
(1)原白色粉末中一定含有
(2)为进一步确定白色粉末中可能含有的物质是否存在,小明设计了如下实验:
(3)写出上述探究过程中任意一个化学方程式
步骤①:取少量白色粉末,加足量水充分溶解后过滤,得到白色沉淀和无色滤液.
步骤②:取步骤①得到的白色沉淀,加入足量稀硝酸,沉淀部分溶解,并有无色气体产生,将气体通入澄清的石灰水中,石灰水变浑浊.
通过分析可知:
(1)原白色粉末中一定含有
CaCO3、Na2SO4和Ba(NO3)2
CaCO3、Na2SO4和Ba(NO3)2
(写化学式,下同),可能含有NaCl
NaCl
.(2)为进一步确定白色粉末中可能含有的物质是否存在,小明设计了如下实验:
| 实验步骤 | 实验目的、现象及结论 |
| 步骤③:取步骤①中的滤液,加入足量的 Ba(NO3)2 Ba(NO3)2 溶液,静置. |
目的是除去滤液中可能还存在的 SO42- SO42- ,排除其干扰. |
| 步骤④:取步骤③中的清液,滴加 HNO3酸化的AgNO3 HNO3酸化的AgNO3 溶液. |
若有白色沉淀生成,则原白色粉末中一定含有该物质;否则不含该物质. |
Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3
Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3
.分析:(1)根据铜离子在溶液中显蓝色,碳酸钙难溶于水,但是会溶于酸,钡离子会与硫酸根离子生成的硫酸钡沉淀难溶于酸进行分析.
(2)依据氯离子一般用硝酸酸化的硝酸银鉴定分析解答即可;
(2)依据氯离子一般用硝酸酸化的硝酸银鉴定分析解答即可;
解答:解:(1)步骤①:取少量白色粉末,加足量水充分溶解后过滤,得到白色沉淀和无色滤液.由于硫酸铜溶液呈蓝色,故一定无硫酸铜;
步骤②:取步骤①得到的白色沉淀,加入足量稀硝酸,沉淀部分溶解,并有无色气体产生,将气体通入澄清的石灰水中,石灰水变浑浊.可以说明生成了二氧化碳.则混合物中一定有碳酸钙,不溶的沉淀则可能是Na2SO4和Ba(NO3)2生成的硫酸钡的沉淀,则固体中一定含有碳酸钠、硫酸钠和硝酸钡,至于是否含有氯化钠无法确定;
(2)步骤③:取步骤①中的滤液,加入足量的硝酸钡以除掉溶液中的硫酸根离子,用以防止产生硫酸银微溶物而影响氯离子的鉴定;
步骤④:取步骤③中的清液,滴加硝酸酸化的硝酸银,如果若有白色沉淀生成(AgCl),则原白色粉末中一定含有该物质;否则不含该物质.
(3)依据以上叙述书写一个相关的方程式即可,如:Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3等;
故答案为:(1)CaCO3、Na2SO4和Ba(NO3)2 ;NaCl;(2)Ba(NO3)2;SO42-;HNO3酸化的AgNO3;Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3;
步骤②:取步骤①得到的白色沉淀,加入足量稀硝酸,沉淀部分溶解,并有无色气体产生,将气体通入澄清的石灰水中,石灰水变浑浊.可以说明生成了二氧化碳.则混合物中一定有碳酸钙,不溶的沉淀则可能是Na2SO4和Ba(NO3)2生成的硫酸钡的沉淀,则固体中一定含有碳酸钠、硫酸钠和硝酸钡,至于是否含有氯化钠无法确定;
(2)步骤③:取步骤①中的滤液,加入足量的硝酸钡以除掉溶液中的硫酸根离子,用以防止产生硫酸银微溶物而影响氯离子的鉴定;
步骤④:取步骤③中的清液,滴加硝酸酸化的硝酸银,如果若有白色沉淀生成(AgCl),则原白色粉末中一定含有该物质;否则不含该物质.
(3)依据以上叙述书写一个相关的方程式即可,如:Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3等;
故答案为:(1)CaCO3、Na2SO4和Ba(NO3)2 ;NaCl;(2)Ba(NO3)2;SO42-;HNO3酸化的AgNO3;Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3;
点评:熟练掌握常见的盐的性质,知道铜盐的溶液为蓝色,而不溶于硝酸的白色沉淀只有硫酸钡和氯化银两种物质是解题的关键;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(1)有一包白色粉末,可能是由硫酸铜、氯化钠、碳酸钠、硫酸钠中的一种或几种组成,为检验其中的成分,经实验得到下表,请完成相关内容.
(2)某化学兴趣小组为测定该包白色粉末中碳酸钠的质量分数,取该样品44.6g,加286.2克水溶解制成溶液后投入146克稀盐酸中完全反应,共收集到二氧化碳气体8.8g.求:(1)该碳酸钠样品中碳酸钠的质量分数;(2)反应所得溶液中溶质的质量分数.
| 实验步骤及现象 | 结论 |
| ①将少许白色粉末溶于水得到无色溶液A | 白色粉末中一定没有 |
| ②在A中加入足量硝酸钡溶液,生成白色沉淀B,过滤得滤液C ③在白色沉淀B中加入足量稀硝酸, ④在滤液C中加入硝酸银溶液,出现白色沉淀,再滴加稀硝酸,沉淀不溶解. |
白色粉末中一定有 碳酸钠和氯化钠 |
 (2013?长宁区二模)有一包白色粉末,可能含有K2SO4、Na2CO3、BaCl2、CuSO4中的一种或几种.取样溶于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,沉淀的质量与加入盐酸体积的关系如图所示.由此推断白色粉末的成分是( )
(2013?长宁区二模)有一包白色粉末,可能含有K2SO4、Na2CO3、BaCl2、CuSO4中的一种或几种.取样溶于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,沉淀的质量与加入盐酸体积的关系如图所示.由此推断白色粉末的成分是( )