题目内容
17.用下列物质的字母序号填空:A.洗衣粉 B.氢气 C.草木灰 D.明矾 E.精肉 F.硫酸铜
(1)不能与铵态氮肥混合施肥的是C; (2)A具有乳化作用;
(3)21世纪的“清洁”能源B; (4)E富含蛋白质;
(5)用于配置波尔多液的是F; (6)D可用于净化水.
分析 根据物质的性质和用途进行分析,洗衣粉中含有乳化剂,具有乳化作用,氢气是清洁能源,草木灰中由于含有碳酸钾而显碱性,明矾可用于净化水,精肉中富含蛋白质,硫酸铜可作为配制波尔多液的原料.
解答 解:(1)碱性物质不能与铵态氮肥混合施用,原因是铵态氮肥能和显碱性的物质反应生成氨气,从而降低肥效,由于草木灰显碱性,故不能与铵态氮肥混合使用;
(2)洗衣粉中含有乳化剂,具有乳化作用;
(3)氢气燃烧只生成水,是清洁能源;
(4)蛋类、豆类、鱼类、奶类、瘦肉类食物中富含蛋白质,所以富含蛋白质的为精肉;
(5)配制波尔多液的原料为硫酸铜、生石灰和水,故用于配置波尔多液的是硫酸铜;
(6)明矾常用于净化水;
故答案为:(1)C (2)A (3)B (4)E (5)F (6)D
点评 本题考查了常见物质的性质及用途,完成此题,可以依据已有的知识进行.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
7.下列化肥中,从外观即可与其他化肥相区别的是( )
| A. | 磷矿粉 | B. | 尿素 | C. | 硫酸钾 | D. | 硝酸铵 |
8.钙及其化合物在生产、生活中具有广泛的应用
(一)钙的广泛用途
(1)高钙奶中含钙,这里的钙是指b.(选填序号,下同)
a.单质 b.元素 c.原子
(2人体中钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其中磷元素化合价为+5.
(3)混凝土中也含有一定量的含钙物质,钢筋与混凝土混合形成钢筋混凝土,以上叙述中不涉及的材料是b.
a.无机材料 b.合成材料 c.复合材料
(二)轻质CaCO3的制备
某实验小组利用石灰石残渣(杂质不溶于水也不溶于酸)制备轻质CaCO3,同时得到K2SO4,流程如图1:

(1)反应Ⅱ中先通NH3,再通CO2的目的是提高二氧化碳的吸收效率,化学方程式为CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4
(2)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是常温下,硫酸钾的溶解度较小.
(3)判断CaCO3固体已洗涤干净的方法是取最后一次洗涤所得的滤液,加入BaCl2溶液,无明显现象;K2SO4晶体洗涤时,不可选用下列A洗涤剂(填字母编号).
A.热水 B.冰水 C.饱和K2SO4溶液
(三)CaSO4•xH2O成分测定
上述流程中分离所得的CaSO4•xH2O中含有一定量的CaCO3.实验小组为了测定CaSO4•xH2O中x的值及含量,取22.20g样品加热至900℃,将得到的气体先通过浓硫酸,再通入碱石灰,测得实验数据如表:
【资料】已知CaSO4•xH2O在160℃生成CaSO4,CaCO3在900℃时分解完全.
(1)CaSO4•xH2O的质量为17.20g
(2)x的值2.
(四)CaSO4•xH2O的性质探究
CaSO4•xH2O受热会逐步失去结晶水,1350℃时 CaSO4开始分解;取纯净CaSO4•xH2O固体3.44g,加热,测定固体质量随温度的变化情况如图2所示.
(1)0~T1固体质量没有发生变化的原因可能是未达到反应所需的温度
(2)G点固体的化学式是CaSO4•H2O.
(3)将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,反应后的固体为氧化物,则
①则H~I段发生反应的化学方程式为2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑;
②m=11.2.
(一)钙的广泛用途
(1)高钙奶中含钙,这里的钙是指b.(选填序号,下同)
a.单质 b.元素 c.原子
(2人体中钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其中磷元素化合价为+5.
(3)混凝土中也含有一定量的含钙物质,钢筋与混凝土混合形成钢筋混凝土,以上叙述中不涉及的材料是b.
a.无机材料 b.合成材料 c.复合材料
(二)轻质CaCO3的制备
某实验小组利用石灰石残渣(杂质不溶于水也不溶于酸)制备轻质CaCO3,同时得到K2SO4,流程如图1:

(1)反应Ⅱ中先通NH3,再通CO2的目的是提高二氧化碳的吸收效率,化学方程式为CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4
(2)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是常温下,硫酸钾的溶解度较小.
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
A.热水 B.冰水 C.饱和K2SO4溶液
(三)CaSO4•xH2O成分测定
| 名称 | 浓硫酸 | 碱石灰 |
| 实验前 | 100.00 | 100.00 |
| 实验后 | 103.60 | 102.20 |
【资料】已知CaSO4•xH2O在160℃生成CaSO4,CaCO3在900℃时分解完全.
(1)CaSO4•xH2O的质量为17.20g
(2)x的值2.
(四)CaSO4•xH2O的性质探究
CaSO4•xH2O受热会逐步失去结晶水,1350℃时 CaSO4开始分解;取纯净CaSO4•xH2O固体3.44g,加热,测定固体质量随温度的变化情况如图2所示.
(1)0~T1固体质量没有发生变化的原因可能是未达到反应所需的温度
(2)G点固体的化学式是CaSO4•H2O.
(3)将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,反应后的固体为氧化物,则
①则H~I段发生反应的化学方程式为2CaSO4$\frac{\underline{\;高温\;}}{\;}$2CaO+2SO2↑+O2↑;
②m=11.2.
5.下列实验现象描述正确的是( )
| A. | 氯化铵和熟石灰混合研磨,闻到刺激性气味 | |
| B. | 打开盛浓盐酸的试剂瓶塞,瓶口上方出现大量白烟 | |
| C. | 镁在空气中燃烧发出耀眼白光,生成氧化镁 | |
| D. | 氢氧化钠溶于水时溶液温度降低 |
12.下列物质放置在空气中一段时间后,能和空气中的水发生化学变化的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 氢氧化钠 | D. | 生石灰 |
2.实验室有一瓶敞口久置的烧碱药品,取20g此样品加水溶解配制成120g溶液,加入氯化钙溶液至恰好完全反应,实验过程如下(不考虑氯化钙与氢氧化钠反应),下列说法正确的是( )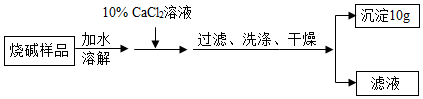

| A. | 滤液中溶质只有氯化钠 | |
| B. | 加入氯化钙溶液的质量为111g | |
| C. | 用氯化钡替代氯化钙所得沉淀质量变大,相对误差偏大 | |
| D. | 样品中氢氧化钠的质量小于9.4g |
9.下列化学用语正确的是( )
| A. | 水银-Ag | B. | 1个氢分子-H2 | C. | 铝-AL | D. | 硫酸铁-FeSO4 |
6.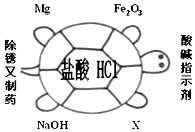 “盐酸化性乌龟壳,一头一尾四只脚”--如图是小王归纳的稀盐酸的化学性质,X的物质类别与图中其他物质不同,则物质X是下列物质中的( )
“盐酸化性乌龟壳,一头一尾四只脚”--如图是小王归纳的稀盐酸的化学性质,X的物质类别与图中其他物质不同,则物质X是下列物质中的( )
 “盐酸化性乌龟壳,一头一尾四只脚”--如图是小王归纳的稀盐酸的化学性质,X的物质类别与图中其他物质不同,则物质X是下列物质中的( )
“盐酸化性乌龟壳,一头一尾四只脚”--如图是小王归纳的稀盐酸的化学性质,X的物质类别与图中其他物质不同,则物质X是下列物质中的( )| A. | 硝酸钾 | B. | 氧化铜 | C. | 碳酸钙 | D. | 氢氧化钾 |