题目内容
7.某化学学习小组在实验室教坛上发现一瓶实验后的混合物质,实验老师说会是以下四种溶液其中两种的混合物H2SO4、KOH、K2SO4、Na2CO3.现由同学去进行验证.(1)猜想可能的组合会是:①H2SO4、K2SO4;②KOH、K2SO4;③KOH、Na2CO3;④K2SO4、Na2CO3.(写出四种可能即可)
(2)为进一步验证,在混合液中加入无色的酚酞,溶液变为红色.由此知混合液中不可能含有H2SO4.
(3)后来化学老师说,根据同学们刚才的实验情况,混合液中应该不含KOH,请同学们通过实验确认化学老师的推断是正确的.
当时教坛上只有硫酸铜溶液、稀硫酸、硝酸银溶液、氯化钡溶液、酚酞溶液、稀盐酸
| 实验操作 | 预期现象与结论 |
分析 根据已有的物质的性质以及物质间反应的实验现象进行分析解答,物质共存则物质间不能反应,酚酞在碱性溶液中变红,在酸性和中性溶液中不变色,据此解答.
解答 解:(1)物质共存则物质间不能反应,故可能是:①H2SO4、K2SO4;②KOH、K2SO4;③KOH、Na2CO3;④K2SO4、Na2CO3;故填:H2SO4、K2SO4;KOH、K2SO4; KOH、Na2CO3;K2SO4、Na2CO3;
(2)在混合液中加入无色的酚酞,溶液变为红色,说明溶液呈碱性,一定不会含有硫酸,故填:H2SO4;
(3)混合液中应该不含KOH,则物质的组成是硫酸钾和碳酸钠,可以加入氯化钡溶液,产生白色沉淀,过滤后向滤液中滴加酚酞试液溶液不变色,说明溶液中不含有碱性物质,即不含有氢氧化钾;故填:
| 实验操作 | 预期现象与结论 |
| 向混合中加入过量的氯化钡溶液,然后过滤,向滤液中滴加酚酞试液 | 产生白色沉淀,滤液不变色 混合液中不含有氢氧化钾 |
点评 本题考查的是物质成分的推断,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
15.某物质在氧气中燃烧,只生成二氧化碳和水,则对该物质的组成叙述正确的是( )
| A. | 一定含碳、氢、氧三种元素 | |
| B. | 一定只含氧元素 | |
| C. | 一定含碳元素和氢元素可能含氧元素 | |
| D. | 一定不含氧元素 |
16.已知KNO3在不同温度下的溶解度如下表:
下列说法不正确的是( )
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| 溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
| A. | 20℃时,把20gKNO3投入100g水中,所得溶液的溶质质量分数为20% | |
| B. | KNO3的溶解度随温度升高而增大 | |
| C. | 30℃时,在100g水中加入45.8g KNO3形成饱和溶液 | |
| D. | 40℃时饱和 KNO3溶液,降温可使它变浓 |
9.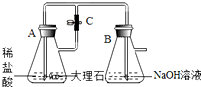 某化学实验小组的同学利用如图所示装置进行实验.A中反应开始时,弹簧夹C处于打开状态.一段时间后,关闭C,装置A中仍在反应.过一会儿,观察到装置A中液体通过长导管进入装置B,装置B中出现白色沉淀,装置A中液体能进入装置B的原因:关闭止水夹C后,A中产生的二氧化碳气体使A气压增大,大于大气压,将A中液体通过长导管压入B中,装置B中出现白色沉淀的化学反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓.小组同学探究反应后装置B中的溶液的溶质成分.
某化学实验小组的同学利用如图所示装置进行实验.A中反应开始时,弹簧夹C处于打开状态.一段时间后,关闭C,装置A中仍在反应.过一会儿,观察到装置A中液体通过长导管进入装置B,装置B中出现白色沉淀,装置A中液体能进入装置B的原因:关闭止水夹C后,A中产生的二氧化碳气体使A气压增大,大于大气压,将A中液体通过长导管压入B中,装置B中出现白色沉淀的化学反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓.小组同学探究反应后装置B中的溶液的溶质成分.
【提出问题】反应后装置B溶液的溶质成分是什么?
【猜想与假设】
猜想1:NaCl、HCl; 猜想2:NaCl、CaCl2;
猜想3:NaCl、NaOH; 猜想4:NaCl、NaOH、Na2CO3.
【交流讨论】经讨论,大家一致认为猜想1一定不合理.理由是若存在HCl会与B中的白色沉淀CaCO3发生反应.
【实验探究】将反应后装置B中所得混合物过滤,取少量滤液分别进行如下实验:
实验1:向滤液中滴加碳酸钠溶液,无明显现象,则猜想2不正确.
实验2:(在下表中横线A、B处填写恰当的内容.)
【反思评价】实验结束后,同学们经过交流与讨论后认为:探究反应后所得溶液的溶质成分时,不仅要考虑生成物还要考虑反应物是否过量.
 某化学实验小组的同学利用如图所示装置进行实验.A中反应开始时,弹簧夹C处于打开状态.一段时间后,关闭C,装置A中仍在反应.过一会儿,观察到装置A中液体通过长导管进入装置B,装置B中出现白色沉淀,装置A中液体能进入装置B的原因:关闭止水夹C后,A中产生的二氧化碳气体使A气压增大,大于大气压,将A中液体通过长导管压入B中,装置B中出现白色沉淀的化学反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓.小组同学探究反应后装置B中的溶液的溶质成分.
某化学实验小组的同学利用如图所示装置进行实验.A中反应开始时,弹簧夹C处于打开状态.一段时间后,关闭C,装置A中仍在反应.过一会儿,观察到装置A中液体通过长导管进入装置B,装置B中出现白色沉淀,装置A中液体能进入装置B的原因:关闭止水夹C后,A中产生的二氧化碳气体使A气压增大,大于大气压,将A中液体通过长导管压入B中,装置B中出现白色沉淀的化学反应方程式为Na2CO3+CaCl2═2NaCl+CaCO3↓.小组同学探究反应后装置B中的溶液的溶质成分.【提出问题】反应后装置B溶液的溶质成分是什么?
【猜想与假设】
猜想1:NaCl、HCl; 猜想2:NaCl、CaCl2;
猜想3:NaCl、NaOH; 猜想4:NaCl、NaOH、Na2CO3.
【交流讨论】经讨论,大家一致认为猜想1一定不合理.理由是若存在HCl会与B中的白色沉淀CaCO3发生反应.
【实验探究】将反应后装置B中所得混合物过滤,取少量滤液分别进行如下实验:
实验1:向滤液中滴加碳酸钠溶液,无明显现象,则猜想2不正确.
实验2:(在下表中横线A、B处填写恰当的内容.)
| 实验操作 | 先向滤液中加入过量Ba(NO3)2溶液 | 然后再向滤液中滴加酚酞溶液 |
| 实验现象 | 出现白色沉淀 | 溶液变红 |
| 实验结论 | 猜想4正确 | |


 、
、 两者关系是B.(填字母)A.同种元素 B.不同种元素.
两者关系是B.(填字母)A.同种元素 B.不同种元素.