题目内容
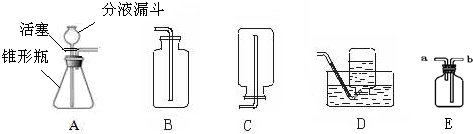
过氧化氢溶液在二氧化锰的条件下能迅速分解成氧气和水。分液漏斗可以通过调节活塞控制液体滴加速度。回答下列问题:

(1)分液漏斗中应放入的物质是 ,锥形瓶中应放入的物质是 。
(2)要收集一瓶纯净的氧气应选择上图中的装置 (填字母)。
(3)某同学在观察到锥形瓶内有大量气泡时,开始用C装置收集氧气, 过一断时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃。其可能原因是 。
(4)为检验装置B中氧气是否收集满,可用带火星的木条放在集气瓶的______,这是利用了氧气___的性质。
(5)若实验时用此法代替高锰酸钾加热制氧气,优点是 (填序号)
A.生成物中只有氧气 B.不需加热 C.需加热
(6)装置A中反应剧烈,据此提出实验安全注意事项是 。
A.控制液体的滴加速度 B.用体积小的锥形瓶 C.加热反应物
(1)过氧化氢溶液 二氧化锰 (2)D (3)装置漏气 (其他合理答案均可)
(4)瓶口 支持燃烧 (5) B (6)A
【解析】(1)分液漏斗装液体药品,应为过氧化氢溶液,则锥形瓶中装二氧化锰.
(2)要收集纯净的氧气应选择排水法,收集干燥的气体才用排空气法.
(3)氧气密度比空气大,用向上排空气法才能收集到氧气.
(4)氧气能支持燃烧,所以检验装置中氧气是否收集满,可用带火星的木条放在集气瓶的瓶口
(5)高锰酸钾制氧气需加热,而过氧化氢常温下就可分解.
(6)A、控制液体的滴加速度,使气流平稳生成,可防装置爆炸;
B、用体积小的锥形瓶,使迅速生成的气体在有限空间内易发生爆炸或使液体喷出,造成危险;
C、加热反应物,也使反应更加剧烈,不能采用.

 过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水.分液漏斗可以通过调节活塞控制液体滴加速度.回答下列问题
过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水.分液漏斗可以通过调节活塞控制液体滴加速度.回答下列问题