题目内容
17.某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16克放入烧杯,把80克稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,也不与稀盐酸反应).请计算:| 序号 | 加入稀盐酸的质量/克 | 剩余固体的质量/克 |
| 第一次 | 20 | 11 |
| 第二次 | 20 | 6 |
| 第三次 | 20 | 2.8 |
| 第四次 | 20 | n |
(2)样品中碳酸钙的质量分数为82.5%.
(3)小明同学计算所用盐酸的溶质质量分数,计算过程如下:
解:设盐酸的溶质质量分数为x
CaCO3+2HCl=CaCl2+H20+C02↑
100 73
13.2g 80x
100:73=13.2:80x
x=12%
小明的计算过程中存在明显错误,你能通过列式计算进行纠正吗?18.25%.
分析 (1)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,而第3次反应后固体物质减少的质量为3.2g,说明此时碳酸钙已反应完,不再产生气体,故表中n的数值为2.8;
(2)根据图表数据可知,完全反应后,剩余固体物质的质量为2.8g,石灰石样品的质量减去剩余固体物质的质量就是样品中碳酸钙的质量,然后根据质量分数公式计算即可;
(3)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,说明20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应.根据碳酸钙与盐酸反应的化学方程式和第1次完全反应中碳酸钙的质量,即可计算出第一次参与反应的HCl质量,然后根据溶质的质量分数公式计算即可.
解答 解:(1)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5g,而第3次反应后固体物质减少的质量为3.2g,说明此时碳酸钙已反应完,不再产生气体,所以表中n的数值为2.8;
(2)样品中碳酸钙的质量分数为:$\frac{16g-2.8g}{16g}$×100%=82.5%;
答:样品中碳酸钙的质量分数为82.5%;
(4)由试题分析20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应,
设第一次参与反应的HCl质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
5g x
$\frac{100}{5g}$=$\frac{73}{x}$
x=3.65g,
盐酸中溶质的质量分数为:$\frac{3.65g}{20g}$×100%=18.25%.
故答案为:(1)2.8;
(2)82.5%;
(3)18.25%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
8.小明通过对电解水生成的两种气体性质的检验,得出与文献一致的结果--两电极上分别产生氢气和氧气.但测得的数据(如下表)却不是文献上的2:1.
于是小明对每一时段产生的气体的量进行了仔细分析,试图找出哪一时段出了问题,结果发现,并不是所有时段产生气体的体积比都不是2:1.
(1)请你也仔细分析一下以上实验数据,能够从中发现的规律是:前4分钟产生的氢气与氧气的体积比大于2:1;从第4分钟开始到第10分钟产生的氢气与氧气的体积比等于2:1.造成其中一时段气体体积比不是2:1的可能原因是氧气的溶解度比氢气的大.
(2)针对上述分析,小明对实验进行了改进,结果得到了满意的结果.你认为小明应该如何改进在电解前给阳极的水通氧使之达到饱和.
(3)请你根据水电解生成氢、氧两种气体以及体积比为2:1的结果推导出水的化学式(如需计算,写出过程.已知:氢气中只有氢元素,氧气中只有氧元素;该实验条件下,氧气的密度为1.44g/L,氢气的密度为0.09g/L):H2O.
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极上产生的气体体积/cm3 | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极上产生的气体体积/cm3 | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
(1)请你也仔细分析一下以上实验数据,能够从中发现的规律是:前4分钟产生的氢气与氧气的体积比大于2:1;从第4分钟开始到第10分钟产生的氢气与氧气的体积比等于2:1.造成其中一时段气体体积比不是2:1的可能原因是氧气的溶解度比氢气的大.
(2)针对上述分析,小明对实验进行了改进,结果得到了满意的结果.你认为小明应该如何改进在电解前给阳极的水通氧使之达到饱和.
(3)请你根据水电解生成氢、氧两种气体以及体积比为2:1的结果推导出水的化学式(如需计算,写出过程.已知:氢气中只有氢元素,氧气中只有氧元素;该实验条件下,氧气的密度为1.44g/L,氢气的密度为0.09g/L):H2O.
2.生活中的下列现象,用分子的相关知识解释错误的是( )
| A. | 水沸腾时能掀起壶盖,说明分子大小随温度升高而增大 | |
| B. | 液化石油气须加压后贮存在钢瓶中,说明分子之间有间隙 | |
| C. | 湿衣服晾在太阳底下干得快,说明分子热运动激烈程度与温度有关 | |
| D. | 成熟的菠萝蜜会散发出浓浓的香味,说明分子在不断地做无规则运动 |
9.有关分子、原子的说法正确的是( )
| A. | 花香四溢说明分子间有间隔 | |
| B. | 原子是化学变化中的最小粒子 | |
| C. | 气体易被压缩是因为气体分子受压变小 | |
| D. | 化学变化中分子、原子都可分 |
6.①开发新能源,减少化石燃料的燃烧;②开发生产无汞电池;③分类回收垃圾;④不提倡使用一次性发泡塑料餐具和塑料袋;⑤提倡使用手帕,减少餐巾纸的使用;⑥提倡不使用含磷洗衣粉;⑦农业上控制化肥和农药的使用.上述措施是为了保护环境的有( )
| A. | ①②③④⑥⑦ | B. | ②③④⑤⑥⑦ | C. | ①②③⑤⑥⑦ | D. | 全部 |
7.在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究,请你参与他们的探究并回答问题.
【猜想】猜想I:红色粉末是铜粉;猜想Ⅱ:红色粉末是氧化铁粉;猜想Ⅲ:红色粉末是铜粉和氧化铁粉的混合物
【实验】经过查阅资料、回忆已学过的知识,
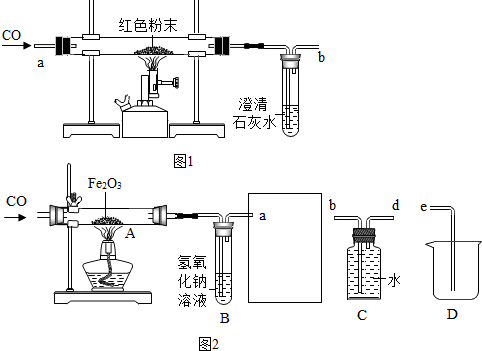
大家决定设计如图1所示的实验进行探究.请完成下列表格:
【表达】通过实验及分析,确定红色粉末是铜粉和氧化铁粉的混合物,则在上述实验过程中所发生反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2、-.
【反思】从环保角度看,图1所示的实验装置有不足之处,请说出其中一种改进方法:在b处用酒精灯点燃,或用塑料袋(气球)收集.
【拓展】为了进一步探究铁和铜的金属活动性强弱,你认为可选用下列试剂中的ABC(填序号).
A.硝酸铜溶液 B.稀盐酸 C.氯化亚铁溶液 D.硫酸镁
【应用】同学们用一氧化碳与氧化铁的反应来模拟炼铁的原理,装置如图2所示,请回答有关问题:
(1)B装置中氢氧化钠溶液的作用是吸收混合气体中的二氧化碳
(2)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→d→b→e.

【猜想】猜想I:红色粉末是铜粉;猜想Ⅱ:红色粉末是氧化铁粉;猜想Ⅲ:红色粉末是铜粉和氧化铁粉的混合物
【实验】经过查阅资料、回忆已学过的知识,
大家决定设计如图1所示的实验进行探究.请完成下列表格:
| 实验中可能出现的现象 | 结论 |
| 红色粉末不变色,石灰水不变浑浊 | 猜想Ⅰ正确 |
| 红色粉末全部变为黑色,石灰水变浑浊 | 猜想Ⅱ正确 |
| 红色粉末部分变为黑色,石灰水变浑浊 | 猜想Ⅲ正确 |
【反思】从环保角度看,图1所示的实验装置有不足之处,请说出其中一种改进方法:在b处用酒精灯点燃,或用塑料袋(气球)收集.
【拓展】为了进一步探究铁和铜的金属活动性强弱,你认为可选用下列试剂中的ABC(填序号).
A.硝酸铜溶液 B.稀盐酸 C.氯化亚铁溶液 D.硫酸镁
【应用】同学们用一氧化碳与氧化铁的反应来模拟炼铁的原理,装置如图2所示,请回答有关问题:
(1)B装置中氢氧化钠溶液的作用是吸收混合气体中的二氧化碳
(2)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→d→b→e.
 在科学学习中使用模型可以反映客观现象,简单明了地表示事物.如图:
在科学学习中使用模型可以反映客观现象,简单明了地表示事物.如图: