题目内容
【题目】取12.5 g石灰石于装置A中,向其中加入100 g足量的稀盐酸,充分反应后(杂质不参加反应),A中固液混合物的质量为108.1 g,请计算:
(1)产生气体的质量_________。
(2)该石灰石中碳酸钙的质量分数_______。
(3)充分反应后溶液中溶质的质量分数_______?
【答案】4.4g 80% 10.5%
【解析】
(1)根据质量守恒定律,二氧化碳的质量为:100g+12.5g-108.1g=4.4g,故填:4.4g;
(2)设该石灰石样品中碳酸钙的质量分数为x,生成氯化钙的质量为y,
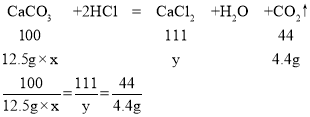
解得x=0.8,y=11.1g
答:该石灰石样品中碳酸钙的质量分数为80%。
(3)充分反应后溶液中溶质的质量分数为:![]()
答:充分反应后溶液中溶质的质量分数为10.5%。

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
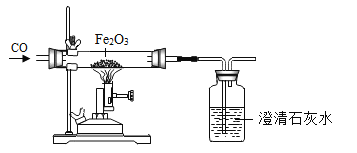
【题目】兴趣小组用如下装置,进行有关碳及其氧化物的化学性质研究(图中夹持仪器已略)。

实验目的 | 实验现象 | 实验分析 |
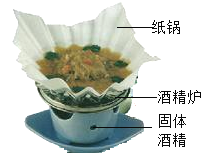
①连接装置AD,探究碳的化学性质。 | A中固体逐渐减少。 | A中化学方程式_____, D中酒精灯的作用_____。 |
②连接装置ABCEF,探究一氧化碳的化学性质。 | B中现象_____。 E中现象_____。 | B中化学方程式_____, C的作用_____, E的作用_____。 |
【题目】不同温度时,NaCl固体的溶解度如下表所示。20℃时,将50g NaCl固体加入到盛有100g水的烧杯中,充分溶解得到溶液。下列说法正确的是
温度/℃ | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |

A.烧杯中溶液的质量为150g
B.烧杯中剩余固体的质量为14g
C.溶液中溶质质量分数的计算式为![]() ×100%
×100%
D.升高温度能将烧杯中的饱和溶液变为不饱和溶液