题目内容
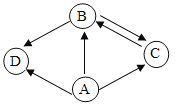
【题目】实验室用如图装置模拟炼铁。下列说法正确的是
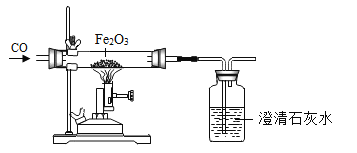
A.该反应属于置换反应
B.应先加热Fe2O3,再通入CO
C.红棕色的Fe2O3粉末逐渐变黑
D.气体通过澄清石灰水后直接排放
【答案】C
【解析】
如图装置模拟炼铁,一氧化碳和三氧化二铁在高温条件下反应生成二氧化碳和铁,则有:
A、置换反应指的是单质与化合物反应生成新的单质与新的化合物的反应,该反应不属于置换反应,A选项不正确,不符合题意;
B、应通入CO,排出装置内的空气,再加热Fe2O3,这样可以防止一氧化碳与空气混合加热发生爆炸的危险,B选项不正确,不符合题意;
C、铁粉为黑色,随着反应的进行红棕色的Fe2O3粉末逐渐变黑,C选项正确,符合题意;
D、尾气中可能有未反应的一氧化碳气体,因此气体通过澄清石灰水后不能直接排放,还要设置尾气处理装置,可以加一个燃着的酒精灯,D选项不正确,不符合题意。故选C。

【题目】现有A、B两种银白色的金属,某同学想要探究这两种金属的活动性。
(设计实验)取大小相同的两块金属,用砂纸打磨光亮,分别放入两支试管中再加入等量的同种稀盐酸,操作与现象如下:
实验 | 试管1 | 试管2 |
操作 |
|
|
现象 | 金属表面产生气泡较慢 | 金属表面产生气泡较快 |
(思考结论)
(1)通过上述实验,判断出两种金属的活动性顺序是A___(填“>”或“<”)B。
(2)假设其中的一种金属是铁,除观察到铁的表面有气泡产生外,还能观察到反应后的溶液呈________(填“浅绿色”或“黄色”),反应的化学方程式为_______。
(3)实验前用砂纸打磨金属片的目的是__________。
(4)如果两种金属是镁和铁,还可以用镁和一种化合物的溶液来证明两者的金属活动性强弱,你认为该化合物可以是_________(填化学式)。
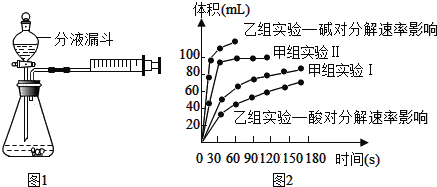
【题目】现甲、乙两化学小组安装两套如图1相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
(1)写出上述反应的化学方程式为_____。
(2)甲、乙小组设计如下实验设计方案。
实验编号 | 温度 | 等质量的催化剂 | 浓度 |
甲组实验I | 25℃ | 0.5g二氧化锰 | 10mL3.49%H2O2 |
甲组实验Ⅱ | 25℃ | 0.5g二氧化锰 | 10mL6.8%H2O2 |
实验编号 | 温度 | 等质量的催化剂 | 浓度 | 加入等浓度的试剂(各2mL) |
乙组实验I | 25℃ | 0.5g二氧化锰 | 10mL6.8%H2O2 | 氢氧化钠 |
乙组实验Ⅱ | 25℃ | 0.5g二氧化锰 | 10mL68%H2O2 | 硫酸 |
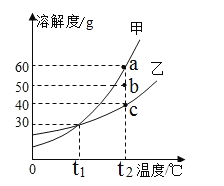
最终实验得到的结果如图2所示,回答下列问题:
①通过甲组实验得出的数据分析,得到的结论是_____;
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析:相同条件下,H2O2在_____(填“酸”或“碱”)性环境下放出气体速率较快。
(3)下列有关H2O2溶液,说法中不正确的是(____)
A H2O2溶液是混合物
B 5.1%的H2O2溶液中氢元素的质量分数为0.3%
C 二氧化锰并不是H2O2分解唯一的催化剂
D H2O2中氢分子和氧分子的个数比为1:1
(4)医学上常用过氧化氢溶液来清洗创口和局部抗菌。为了测定一瓶医用过氧化氢水溶液的溶质质量分数,取该过氧化氢溶液68.0g放入烧杯中然后称量得到108.8g,然后加入2.0g二氧化锰,完全反应后,再称量其质量为110.0g。请回答下列问题:
①生成的氧气为_____g;蒸干烧杯内液体,所得固体物质为_____g。
②试通过计算求该过氧化氢溶液中溶质的质量分数。_____(要有计算过程,结果精确到0.1%)