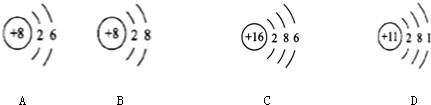题目内容
16.某课外兴趣小组的同学绘制四种实验室操作的变化趋势图象,其中正确的是( )
①将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
②常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸充分反应
③向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量
④高温煅烧一定质量的碳酸钙
⑤分别向等质量的镁和铁中滴入溶质质量分数相同稀盐酸至过量.
| A. | ②③④ | B. | ③④⑤ | C. | ③④ | D. | ③ |
分析 看图象一般看图象的起点、终点、转折点、走势,然后结合每个选项的内容并和图象进行对照.
①将一定质量的硝酸钾不饱和溶液恒温蒸发水分,其质量分数不断增大,有晶体析出后质量分数不再改变;
②根据两种金属的活动性顺序和相对原子质量的大小关系进行分析;
③根据酸碱盐的混合溶液中,中和反应优先的原则进行分析;
④根据高温煅烧石灰石生成二氧化碳和氧化钙,进行分析;
⑤根据金属与酸反应产生气体的多少分析;
解答 解:①随着水分的蒸发,质量肯定会增大,但是当溶液达到饱和溶液以后,质量分数就会保持不变,故①错误.
②在金属性活动顺序表中,锌排在铁的前面,所以锌和稀硫酸的反应速率大于铁,所以在图象中锌的图象更靠近纵坐标,故②错误.
③氢氧化钠先和硫酸反应生成硫酸钠和水,因此刚开始没有沉淀;等硫酸反应后,氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,等反应完全后,沉淀的质量就保持不变,故③正确.
④高温煅烧石灰石生成二氧化碳和氧化钙,固体的质量减少,当碳酸钙分解完毕时固体质量不再改变,但钙元素质量不变,所以钙元素质量分数先逐渐变大,当碳酸钙分解完毕时,钙元素质量分数不再改变,故④正确;
⑤等质量的金属镁和铁中分别滴入溶质质量分数相等的稀盐酸至过量,开始时金属过量,稀盐酸完全反应,生成氢气的质量相同;当向等质量的镁和锌中加入溶质质量分数相同的稀盐酸至过量,则镁和锌全部参加反应,
Mg+2HCl═MgCl2+H2↑
24 2
Fe+2HCl═FeCl2+H2↑
56 2
通过反应的化学方程式以及金属与酸反应生成氢气的质量关系可以看出,镁生成的氢气大于铁,故⑤正确;
故选:B.
点评 本题通过图象考查化学定量性变化过程,既要对化学反应原理清楚,又要对图象从多角度观察,以达到快速准确的解题.解图象类型的试题一般可从两方面解题:一方面从化学反应原理分析入手;二方面抓住图象的三个点即起点、转折点、终点是否正确.

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案| A. | 酒精用于给发烧病人擦拭以降低体温 | |
| B. | 天然气用作燃料 | |
| C. | 液氮用作冷冻剂 | |
| D. | 银用于制作导线 |
(1)由于人的胃里有HCl(填化学式),因此胃液分泌过多会引起胃病,服用含有氢氧化铝的药物可缓解病痛的原理是(用化学方程式表示)3HCl+Al(OH)3=AlCl3+3H2O.
(2)人被昆虫叮咬后皮肤红肿起泡,这是由于昆虫在皮肤内注入了少量甲酸(一种酸性物质)所致.把少许下表所列的生活常用品AC(填编号)涂在被咬的皮肤上,痛痒会消失.
| 物质 | A | B | C | D |
| 肥皂水 | 食醋 | 牙膏 | 食盐水 | |
| pH | 10 | 3 | 9 | 7 |
 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
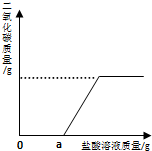
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的
质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
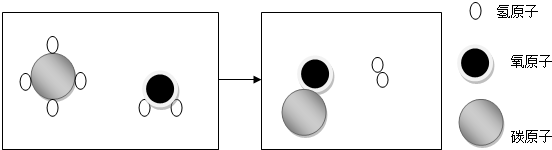
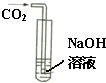 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳气体通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究:探究一:二氧化碳与氢氧化钠是否发生了反应?
同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡冒出,证明二氧化碳与氢氧化钠发生了反应.
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】
佳佳认为:溶质是Na2CO3
贝贝认为:溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性.
【实验验证】
贝贝为了验证自己的猜想,进行如下实验,请你补充完整
| 实验操作 | 实验现象 | 结论 |
| ①取一定量大试管中的溶液于试管中,滴加过量CaCl2溶液,过滤. ②向滤液中滴加酚酞 | 溶液变成红色 | 贝贝的猜想成立 |
(1)贝贝滴加过量CaCl2溶液的目的是把碳酸钠充分反应
(2)贝贝过滤后的滤液中的溶质是氢氧化钠
【实验反思】
同学们联想到氢氧化钠溶液与稀硫酸发生中和反应时也观察不到明显现象,为了验证反应确实发生了,有同学设计了如下实验方案:先用pH试纸测定NaOH 溶液的pH,再向其中滴加稀硫酸,边滴边测定混合溶液的pH,当测得pH小于或等于7时,便可证明反应发生了.
请你分析上述方案中,为什么要“当测得pH小于或等于7时”,才能证明反应发生了,原因是排除因硫酸的加入,稀释氢氧化钠溶液而引起pH减小因素的干扰.
| A. | 热敷袋中的活性炭会达到着火点而燃烧 | |
| B. | 热敷袋主要利用铁生锈放热 | |
| C. | 发热剂需接触空气才会发热 | |
| D. | 食盐能加快热敷袋中铁生锈的速度 |
| A. | CO和CO2都能溶于水生成酸 | |
| B. | CO有还原性,可用于冶炼金属 | |
| C. | CO2的过多排放不会导致酸雨的产生 | |
| D. | CO与CO2 可用澄清石灰水区分 |