题目内容
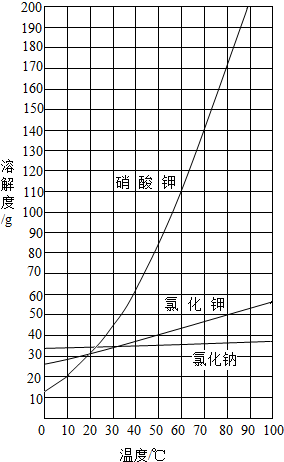 如图是部分固体物质的溶解度曲线.请回答:
如图是部分固体物质的溶解度曲线.请回答:(1)下列说法中错误的是
AB
AB
(填A、B、C符号) A.硝酸钾的溶解度大于氯化钠的溶解度
B.硝酸钾与氯化钾的溶解度相等
C.图中所列物质的溶解度都随温度的升高而增大
(2)80°C时,100g水中溶解40g氯化钾,所形成的溶液是
不饱和
不饱和
溶液(填“饱和”或“不饱和”);(3)在实验室将硝酸钾和氯化钠的热混合溶液(两者均已达饱和)冷却至室温,有晶体析出,析出的晶体中主要物质是
硝酸钾
硝酸钾
.分析:(1)比较物质的溶解度须确定温度,由溶解度曲线可知物质的溶解度随温度变化情况;
(2)据该温度下物质的溶解度分析解答;
(3)硝酸钾的溶解度受温度的影响较大,氯化钠的溶解度受温度影响较小,所以冷却其热饱和溶液析出的晶体主要是硝酸钾.
(2)据该温度下物质的溶解度分析解答;
(3)硝酸钾的溶解度受温度的影响较大,氯化钠的溶解度受温度影响较小,所以冷却其热饱和溶液析出的晶体主要是硝酸钾.
解答:解:(1)比较物质的溶解度须确定温度,故AB错误,由溶解度曲线可知三种物质的溶解度都随温度的升高而增大,不过变化的幅度不同;
(2)80°C时,氯化钠的溶解度是50g,所以100g水中溶解40g氯化钾,所形成的溶液是不饱和溶液;
(3)硝酸钾的溶解度受温度的影响较大,氯化钠的溶解度受温度影响较小,所以在实验室将硝酸钾和氯化钠的热混合溶液(两者均已达饱和)冷却至室温,析出的晶体中主要物质是硝酸钾;
故答案为:(1)AB; (2)不饱和; (3)硝酸钾.
(2)80°C时,氯化钠的溶解度是50g,所以100g水中溶解40g氯化钾,所形成的溶液是不饱和溶液;
(3)硝酸钾的溶解度受温度的影响较大,氯化钠的溶解度受温度影响较小,所以在实验室将硝酸钾和氯化钠的热混合溶液(两者均已达饱和)冷却至室温,析出的晶体中主要物质是硝酸钾;
故答案为:(1)AB; (2)不饱和; (3)硝酸钾.
点评:本题考查了学生观察溶解度曲线并利用溶解度曲线解决问题的能力,难度不大.

练习册系列答案
相关题目
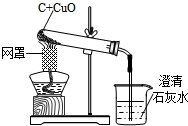 如图是木炭还原氧化铜的探究实验装置.
如图是木炭还原氧化铜的探究实验装置.【提出问题】木炭还原氧化铜产生什么气体?
【提出猜想】产生的气体有三种情况:
①CO;②CO2;③
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,数据设计如下:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | M1 | M2 | △m1即( M1-M2) |
| 烧杯+澄清石灰水 | M3 | M4 | △m2即( M4-M3) |
(2)若猜想②正确,理论上△m1与△m2 的关系是:△m1
【实验并记录】实验得到的数据如下表:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | 69.8g | 65.4g | △m1 |
| 烧杯+澄清石灰水 | 118.8g | 122.6g | △m2 |
【反思与评价】经查阅资料知道:木炭还原氧化铜产生CO2气体,该反应的化学方程式为:
本次实验结果与资料显示不一致.对其可能原因有同学提出下列分析,其中合理的是
A.装置漏气 B.生成的CO2部分与过量的C反应生成了CO
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收.
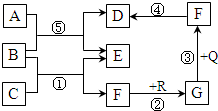 (2012?十堰模拟)如图是初中化学物质间的转化关系(部分反应条件和产物略去),其中F是参加绿色植物光合作用的气体,Q、R都是黑色固体,R在高温条件下与F反应只生成G,E是两种元素组成的钾盐.
(2012?十堰模拟)如图是初中化学物质间的转化关系(部分反应条件和产物略去),其中F是参加绿色植物光合作用的气体,Q、R都是黑色固体,R在高温条件下与F反应只生成G,E是两种元素组成的钾盐.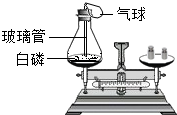
 如图是部分固体物质的溶解度曲线.请回答:
如图是部分固体物质的溶解度曲线.请回答: