题目内容
三氧化铬(CrO3)常用于金属镀铬.在工业上,用重铬酸钠(Na2Cr2O7)制造三氧化铬,反应的化学方程式:Na2Cr2O7+H2SO4=2CrO3+Na2SO4+X,其中X的化学式是 ,在CrO3中Cr元素的化合价是 .
考点:质量守恒定律及其应用,有关元素化合价的计算
专题:化学式的计算,化学用语和质量守恒定律
分析:由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
根据在化合物中正负化合价代数和为零,结合CrO3的化学式进行解答.
根据在化合物中正负化合价代数和为零,结合CrO3的化学式进行解答.
解答:解:根据反应的化学方程式Na2Cr2O7+H2SO4=2CrO3+Na2SO4+X,反应物中钠、铬、氧、氢、硫原子个数分别为2、2、11、2、1,反应后的生成物中钠、铬、氧、氢、硫原子个数分别为2、2、10、0、1,根据反应前后原子种类、数目不变,则每个X分子由2个氢原子和1个氧原子构成,则物质X的化学式为H2O.
氧元素显-2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×3=0,则x=+6价.
故答案为:H2O;+6.
氧元素显-2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×3=0,则x=+6价.
故答案为:H2O;+6.
点评:本题难度不大,利用化学反应前后原子守恒来确定物质的化学式的方法、利用化合价的原则计算指定元素的化合价的方法是正确解答本题的关键.

练习册系列答案
相关题目
下列方法中不能用于鉴别二氧化碳与氧气的是( )
| A、紫色石蕊试液 |
| B、灼热的氧化铜 |
| C、澄清石灰水 |
| D、燃着的小木条 |
下列说法正确的是( )
| A、因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 |
| B、因为SO2和SO3的组成元素相同,所以它们的化学性质相同 |
| C、因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有C和H |
| D、因为CO具有可燃性,所以CO可以用来炼铁 |
鉴别下列物质所使用的方法或试剂,错误的是( )
| A、二氧化碳与氨气:燃着的木条 |
| B、氯化钠与碳酸钠:无色酚酞 |
| C、黄铜与黄金:稀盐酸 |
| D、氢化钾与氯化铵:熟石灰 |
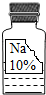 实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).
实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示). 某学习小组用相同的光亮铁钉探究铁生锈与哪些因素有关,设计的实验如图所示:
某学习小组用相同的光亮铁钉探究铁生锈与哪些因素有关,设计的实验如图所示: