题目内容
13.点燃氢气前先要检验它的纯度,制取氧气前先要检验装置的气密性,氢气是理想燃料的原因氢气在空气里的燃烧,实际上是与空气里的氧气发生反应,生成水,没有废气产生.分析 根据可燃性气体容易发生爆炸的原理、氧气的制取和氢气的用途来考虑本题.
解答 解:点燃可燃性气体和空气(或者氧气)的混合物,都易发生爆炸,只要在它的爆炸极限之内,就能爆炸,所以点燃氢气前一定要检验它的纯度,制取氧气前先要检验装置的气密性,氢气是理想燃料的原因氢气在空气里的燃烧,实际上是与空气里的氧气发生反应,生成水,没有废气产生;
故答案为:检验它的纯度;检验装置的气密性;氢气在空气里的燃烧,实际上是与空气里的氧气发生反应,生成水,没有废气产生.
点评 了解点燃可燃性气体和空气(或者氧气)的混合物,都易发生爆炸,所以点燃可燃性气体前一定要检验它的纯度.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
3.下列是几种粒子的结构示意图,其中表示阳离子的是( )
| A. |  | B. |  | C. |  | D. |  |
4.某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
(1)催化剂的种类与过氧化氢溶液分解速率是否有关呢?甲设计以下对比实验:
Ⅰ.将3.0g10%H2O2溶液与1.0gMnO2均匀混合;
Ⅱ.将xg10%%H2O2溶液与1.0gCuO均匀混合.
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
Ⅱ中x的值应为3.0g.
(2)乙探究了影响过氧化氢溶液分解速度的某种因素,实验数据记录如下:
本实验中,测量O2体积的装置是C(填编号)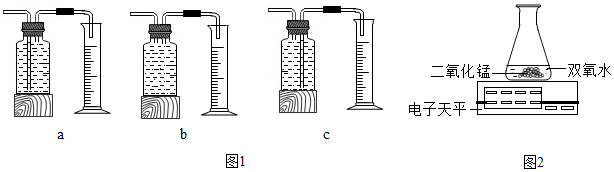
实验结论:在相同条件下,过氧化氢溶液浓度越高,过氧化氢溶液分解得越快.
(3)丙用如图2装置进行实验,通过比较相同时间内反应前后天平的读数之差也能达到实验目的.
(1)催化剂的种类与过氧化氢溶液分解速率是否有关呢?甲设计以下对比实验:
Ⅰ.将3.0g10%H2O2溶液与1.0gMnO2均匀混合;
Ⅱ.将xg10%%H2O2溶液与1.0gCuO均匀混合.
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
Ⅱ中x的值应为3.0g.
(2)乙探究了影响过氧化氢溶液分解速度的某种因素,实验数据记录如下:
| 编号 | 过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | 二氧化锰的质量 | 相同时间内产生氧气的体积 |
| Ⅰ | 50.0g | 1% | 0.1g | 9ml |
| Ⅱ | 50.0g | 2% | 0.1g | 16ml |
| Ⅲ | 50.0g | 4% | 0.1g | 31ml |

实验结论:在相同条件下,过氧化氢溶液浓度越高,过氧化氢溶液分解得越快.
(3)丙用如图2装置进行实验,通过比较相同时间内反应前后天平的读数之差也能达到实验目的.
1.有关分子、原子、元素、物质,下列叙述正确的是( )
| A. | CO2分子是由一个碳原子和一个氧分子构成 | |
| B. | 不同元素的原子核电荷数一定不同 | |
| C. | 核外电子排布相同的粒子一定属于同种元素 | |
| D. | 原子、分子、元素都可构成物质 |
8.在一个密闭容器中放入四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如下表,下列说法不正确的是( )
| 物质 | X | Y | Z | W |
| 反应前质量/g | 2 | 1 | 16 | 16 |
| 反应后质量/g | 17 | n | 6 | 11 |
| A. | 该反应为化合及应 | B. | 物质Y可能是该反应的催化剂 | ||
| C. | 反应后Z和Y的质量比为10:1 | D. | 参加反应的Z和W的质量比为2:1 |
18.我国古代有“女娲补天”的传说,今天,人类也面临“补天”.是指臭氧发生如下变化:3O2$\frac{\underline{\;催化剂\;}}{\;}$2O3,使臭氧层出现空洞,“补天”就是要防止臭氧层出现空洞的形成.下列说法中正确的是( )
| A. | O2和O3都是单质 | B. | O2和O3都是同一种物质 | ||
| C. | O2和O3的性质完全相同 | D. | 该反应是物理变化而不是化学变化 |
5.下列物质的用途只与化学性质有关的是( )
| A. | 用活性炭吸附有毒气体 | |
| B. | 金刚石用于裁玻璃 | |
| C. | 用澄清的石灰水来检验二氧化碳气体 | |
| D. | 用同铜来做导线 |
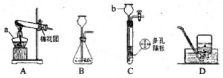 结合图示实验装置,回答下列问题.
结合图示实验装置,回答下列问题.