题目内容
把15.8g高锰酸钾完全分解可制得多少克氧气?若用过氧化氢制取这些氧气,至少需要过氧化氢多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据题目中的反应物、生成物和反应条件,依据化学方程式的书写方法,可以写出高锰酸钾分解的化学方程式;然后由化学方程式找出高锰酸钾和氧气的质量比,由高锰酸钾的质量可计算出生成氧气的质量.
解答:解:设充分反应后生成氧气的质量为x.
2KMnO4
K2MnO4+MnO2+O2↑
316 32
15.8g x
=
x=1.6g
设需要过氧化氢的质量为x
2H2O2
2H2O+O2↑
68 32
x 1.6g
=
x=3.4g
答案:15.8g高锰酸钾完全分解可制得1.6g克氧气,若用过氧化氢制取这些氧气,至少需要过氧化氢3.4克.
2KMnO4
| ||
316 32
15.8g x
| 316 |
| 15.8g |
| 32 |
| x |
x=1.6g
设需要过氧化氢的质量为x
2H2O2
| ||
68 32
x 1.6g
| 68 |
| x |
| 32 |
| 1.6g |
x=3.4g
答案:15.8g高锰酸钾完全分解可制得1.6g克氧气,若用过氧化氢制取这些氧气,至少需要过氧化氢3.4克.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
下列化学仪器的名称书写正确的是( )
| A、锥型瓶 | B、坩锅钳 |
| C、胶头滴管 | D、托盘天枰 |
能够直接在酒精灯火焰上加热的是( )
①试管 ②烧杯 ③量筒 ④蒸发皿 ⑤石棉网.
①试管 ②烧杯 ③量筒 ④蒸发皿 ⑤石棉网.
| A、①④⑤ | B、③② |
| C、①②⑤ | D、①④ |
物质发生化学变化时一定会发生改变的是( )
| A、分子种类 | B、原子种类 |
| C、元素种类 | D、分子数目 |
“黄金搭档”中富含钙、铁、锌、硒、维生素,广告词中的钙、铁、锌、硒指的是( )
| A、原子 | B、物质 | C、离子 | D、元素 |
化学学习小组做实验时记录了下列实验现象,其中正确的是( )
| A、硫在氧气中燃烧发出蓝紫色火焰,生成二氧化硫气体 |
| B、红磷在空气中燃烧,产生大量白色烟雾 |
| C、木炭在氧气中燃烧,发出红色的火焰,产生使澄清石灰水变浑浊的气体 |
| D、细铁丝在氧气中剧烈燃烧,火星四射,有黑色固体生成 |
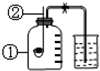 气密性良好的实验装置(如图所示)中仪器①、②的名称分别是
气密性良好的实验装置(如图所示)中仪器①、②的名称分别是