题目内容
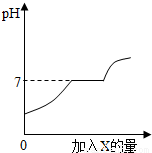
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质 X,溶液的pH随滴入X的量的变化关系如右图所示。则X是

A.水 B.稀盐酸 C.碳酸钠溶液 D.澄清石灰水
【答案】
C
【解析】
试题分析:盐酸和CaCl2的混合溶液呈酸性,若加入水,则溶液的PH将升高,但不会超过7;若加入稀盐酸,则溶液的PH将变小,呈下降趋势;若加入碳酸钠溶液,则碳酸钠先和盐酸反应,溶液PH变大,当碳酸钠与盐酸反应完以后,碳酸钠将与氯化钙反应,此时溶液PH不变,当氯化钙被反应掉以后,碳酸钠过量,溶液PH将增大,超过7;若加入澄清石灰水,则氢氧化钙与盐酸反应,溶液PH变大,一旦盐酸被反应完,则氢氧化钙过量,溶液的PH将立刻大于7,并不断变大。选C。
考点:化学反应中的PH变化图像。
点评:解答本题时,要注意讨论加入物质的量的变化趋势和溶液PH的变化趋势。

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目

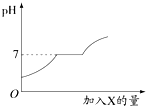 23、现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如右图所示.则X是( )
23、现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如右图所示.则X是( ) (2012?工业园区模拟)现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )
(2012?工业园区模拟)现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )