题目内容
8.同学们为了比较锌、铁、铜三种金属的活动性,仅用组内物质就能达到目的是( )①Zn、Fe、Cu、稀硫酸
②Fe、ZnSO4溶液、CuSO4溶液
③Zn、FeSO4溶液、CuSO4溶液
④Zn、Cu、FeSO4溶液.
| A. | ①②④ | B. | ②和③ | C. | 只有④ | D. | ①②③④ |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.
解答 解:①Zn、Fe均能与稀硫酸反应生成氢气,且锌与稀硫酸反应的速率较快,说明了活动性锌>铁>氢;Cu不与稀硫酸反应,则氢>铜;由此可得出三种金属活动性锌>铁>铜;故该方案合理.
②Fe与ZnSO4溶液不反应,说明了活动性锌>铁;铁与CuSO4溶液反应置换出铜,说明了活动性铁>铜;由此可得出三种金属活动性锌>铁>铜;故该方案合理.
③锌与FeSO4溶液、CuSO4溶液均能发生置换反应,说明了活动性锌>铁,锌>铜,但无法确定铁和铜的活动性强弱,故该方案不合理.
④Zn与FeSO4溶液能发生置换反应,说明了活动性锌>铁;Cu与FeSO4溶液不反应,说明了活动性铁>铜;由此可得出三种金属活动性锌>铁>铜;故该方案合理.
故①②④仅用组内物质就能达到目的.
故选:A.
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.

练习册系列答案
相关题目
18.家庭生活中处处都有物质变化,以下属于物理变化的是( )
| A. | 鲜牛奶变质 | B. | 钢丝球刷碗 | C. | 酵母粉发酵 | D. | 洁厕剂除垢 |
19.下列各组溶液混合(酸均过量),最终无沉淀的是( )
| A. | Na2SO4、Ba(OH)2、H2SO4 | B. | Na2CO3、AgNO3、HCl | ||
| C. | AgNO3、CaCl2、HNO3 | D. | NaOH、MgCl2、H2SO4 |
13.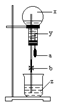 如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )
如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )
 如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )
如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )| x气体 | y液 | z试剂 | |
| ① | O2 | H2SO4 | 紫色石蕊试液 |
| ② | CO2 | NaOH | 无色酚酞试液 |
| ③ | CO | Ca(OH)2 | 无色酚酞试液 |
| ④ | HCl | H2O | 紫色石蕊试液 |
| A. | ②④ | B. | 只有② | C. | ①② | D. | ③④ |
20.现有40g质量分数为10%的食盐溶液,要使其溶质的质量分数达到20%,可采用的方法是( )
①蒸发掉20克水 ②蒸发后溶液中还剩20克水 ③加入3.2克食盐 ④加入5克食盐.
①蒸发掉20克水 ②蒸发后溶液中还剩20克水 ③加入3.2克食盐 ④加入5克食盐.
| A. | ①④ | B. | ①② | C. | ②④ | D. | ①②④ |
17.某同学去我市的某风景区游玩时,取回了若干块矿石样品,他采用了以下的方法对样品中碳酸钙的质量分数进行检测:取这种石灰石样品6克,把40克稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应).
求:(1)6克石灰石样品中含有的杂质为1.2克.
(2)m=2.0.
(3)样品中碳酸钙的质量分数是多少?
(4)所用稀盐酸的质量分数是多少?
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(克) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(克) | 4.0 | m | 1.2 | 1.2 |
(2)m=2.0.
(3)样品中碳酸钙的质量分数是多少?
(4)所用稀盐酸的质量分数是多少?
18.鉴别丝织物是真丝(相当于动物毛发),还是人造丝(有机合成纤维)的方法( )
| A. | 滴入浓硫酸 | B. | 看颜色是否鲜艳 | C. | 灼烧后闻气味 | D. | 无法鉴别 |
 准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如右图所示.试求:
准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如右图所示.试求: