题目内容
6.目前大部分城市居民所使用的燃料主要是管道煤气或天然气,管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4,它们的燃烧反应如下:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
(1)根据以上化学方程式判断,相同条件下,燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是天然气,因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是增大进风口(填“增大”或“减小”),如不改进可能产生的不良后果是天然气不能充分燃烧,可能生成有毒的CO.
(2)家庭煤气管常用硬质聚氯乙烯和聚乙烯塑料管,塑料管属于有机合成材料.
(3)管道煤气中含有的烃类,除甲烷外还有少量乙烷、丙烷、丁烷等的某些性质见表:
| 乙烷 | 丙烷 | 丁烷 | |
| 熔点/℃ | -183.3 | -189.7 | -183.4 |
| 沸点/℃ | -88.6 | -42.1 | -0.5 |
分析 (1)可以根据化学方程式中的微观粒子个数比进行分析解答;
(2)根据材料的分类解答;
(3)根据气体沸点低时容易液化解答.
解答 解:
(1)根据以上三个燃烧方程式可以看出,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
燃烧相同体积的天然气消耗的空气体积较大,因此要保证天然气完全燃烧,燃烧管道煤气的灶具改烧天然气,就必须加大空气进气量,增大进风口.如果不改变就会造成天然气不能充分燃烧而产生大量CO,容易使人中毒或死亡.
(2)家庭煤气管常用硬质聚氯乙烯和聚乙烯塑料管,塑料管属于有机合成材料;
(3)从表中数据可以看出,丁烷的沸点为-0.5℃,在冬天温度较低时容易液化为液体,使管道内气流不畅,因此火焰较小并且呈断续状态.
故答案为:
(1)天然气,增大,天然气不能充分燃烧,可能生成有毒的CO;
(2)有机合成;
(3)丁烷遇冷凝结为液体使管道内气流不畅;
点评 本题考查了化学反应能量变化的分析,主要是反应定量计算的分析判断,题信息的分析应用,掌握基础,审题仔细是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列变化中一定发生了化学变化的是( )
| A. | 水结成冰 | B. | 玻璃破碎 | C. | 石蜡熔化 | D. | 酒精燃烧 |
17. 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )| A. | x的值是15 | B. | 丙可能是该反应的催化剂 | ||
| C. | 该反应是分解反应 | D. | 反应中甲和乙的质量比为4:1 |
14. 如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法 不正确的是( )
如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法 不正确的是( )
 如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法 不正确的是( )
如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法 不正确的是( )| A. | 10℃时,可配制溶质的质量分数均为 20%的甲、乙溶液 | |
| B. | 恒温蒸发溶剂可使接近饱和的甲、乙溶液都变成饱和溶液 | |
| C. | 30℃时,用质量相同的甲、乙分别与足量水配制饱和溶液,结果甲配得的饱和溶液质量大于乙 | |
| D. | 20℃时,将两种饱和溶液混合在一起,所得溶液对两种溶 质而言,均为不饱和溶液 |
1.下列实验操作正确的是( )
| A. |  称量固体 | B. |  固体的取用 | C. |  点燃酒精灯 | D. |  测溶液的pH |
11.河南省实验中学校园的夏天,枇杷路旁橙果簇拥,葡萄长廊碧果串珠.水果主要为人体补充的营养素是( )
| A. | 糖类 | B. | 无机盐 | C. | 维生素 | D. | 油脂 |
18.2017年4月,天舟一号与天宫二号成功完成推进剂在轨补加任务.偏二甲肼(C2H8N2)可用作推动火箭发射的燃料,下列有关其说法正确的是( )
| A. | 偏二甲肼的相对分子质量为60 | |
| B. | 偏二甲肼中碳、氮元素的质量比为1比l | |
| C. | 偏二甲肼中氢元素质量分数最大 | |
| D. | 偏二甲肼分子由C2H8分子和N2分子构成 |
 构建知识网络是一种重要的学习方法.如图D可助消化,A、C属于同类别的化合物,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,完善这个知识网络:
构建知识网络是一种重要的学习方法.如图D可助消化,A、C属于同类别的化合物,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,完善这个知识网络: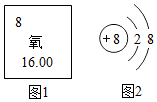 如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图.
如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图.