题目内容
25、现代元素周期表的雏形.下表为元素周期表的部分示意图,请利用下表回答相关问题.

(1)一个水分子共有
(2)我发现如下规律:
①在化学反应中,第Ⅰ纵行的元素比较容易
②从原子结构方面看:同一横行的元素具有相同的
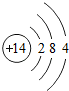
(3)图甲是两种元素在周期表中的信息,图乙是氟原子的原子结构示意图.请完成下列问题:

①图甲方框的横线上填的是
②图甲所示两种元素形成化合物的化学式为

(1)一个水分子共有
3
个原子核、10
个质子.一个Mg2+核外共有10
个电子;Cl-的最外层电子数和Ne或Ar
原子的最外层电子数相同.(2)我发现如下规律:
①在化学反应中,第Ⅰ纵行的元素比较容易
失
电子;第Ⅵ纵行的元素比较容易得
电子,(除H外)都通常达到8个电子的稳定结构.可见元素的化学性质主要决定于原子的最外层电子
数.②从原子结构方面看:同一横行的元素具有相同的
电子层
数;同一纵行的元素具有相同的最外层电子
数.此外还有:同一纵行从上到下电子层数逐渐增加相似的化学性质
;(3)图甲是两种元素在周期表中的信息,图乙是氟原子的原子结构示意图.请完成下列问题:

①图甲方框的横线上填的是
Ca
,图乙方框横线上的数字是7
;②图甲所示两种元素形成化合物的化学式为
CaF2
.分析:根据元素周期表的知识,规律和原子序数,质子数,核外电子数之间的关系元素及化合价知识进行解答本题.
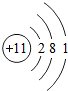
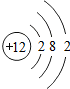
解答:解:(1)一个水分子是H2O,它是由2个H原子和1个O原子构成,共有3个原子,H元素核内有1个质子,O元素核内有8个质子,因此一个水分子有10个质子;Mg2+表示带两个单位正电荷,从元素周期表可查得Mg的原子结构示意图,失去2个电子变成Mg2+,因此核外共有10个电子;Cl-表示带1个单位负电荷,从元素周期表可查得Cl的原子结构示意图,得到1个电子变成Cl-,最外层电子数为8,从元素周期表可查最外层电子数为8的元素有Ne或Ar,故答案为:3;10;10;Ne或Ar;
(2)①在化学反应中,金属元素的原子比较容易失去最外层的电子,非金属元素的原子比较容易得到电子,使最外层通常得到8 个电子的稳定结构,化学元素汉字名称的偏旁可得知第Ⅰ纵行的元素属于金属元素,第Ⅵ纵行的元素属于非金属元素,元素的化学性质由最外层电子数决定,故答案为:失;得;最外层电子;
②根据元素周期表的规律,从原子结构方面看:同一横行的元素具有相同的电子层数;同一纵行从上到下电子层数逐渐增加;同一纵行,原子最外层电子数相同;故答案为:电子层;最外层电子;同一纵行从上到下电子层数逐渐增加;
(3)①根据元素在周期表中的信息,图甲方框的横线上填的是钙元素的元素符号为Ca,在原子中,原子序数=质子数=核外电子数,根据题中元素的原子结构示意图,图乙方框横线上的数字是2+x=9,则x=7;故选Ca;7;
②根据两种元素化合价,形成化合物的化学式为CaF2,故选CaF2.
(2)①在化学反应中,金属元素的原子比较容易失去最外层的电子,非金属元素的原子比较容易得到电子,使最外层通常得到8 个电子的稳定结构,化学元素汉字名称的偏旁可得知第Ⅰ纵行的元素属于金属元素,第Ⅵ纵行的元素属于非金属元素,元素的化学性质由最外层电子数决定,故答案为:失;得;最外层电子;
②根据元素周期表的规律,从原子结构方面看:同一横行的元素具有相同的电子层数;同一纵行从上到下电子层数逐渐增加;同一纵行,原子最外层电子数相同;故答案为:电子层;最外层电子;同一纵行从上到下电子层数逐渐增加;
(3)①根据元素在周期表中的信息,图甲方框的横线上填的是钙元素的元素符号为Ca,在原子中,原子序数=质子数=核外电子数,根据题中元素的原子结构示意图,图乙方框横线上的数字是2+x=9,则x=7;故选Ca;7;
②根据两种元素化合价,形成化合物的化学式为CaF2,故选CaF2.
点评:本题考查学生对元素周期表知识的总结应用能力.

练习册系列答案
相关题目






 表示的是
表示的是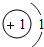
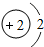
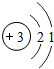
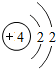
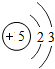
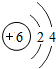
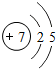
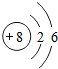
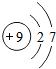
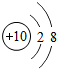
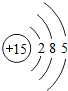
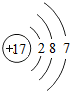
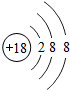
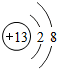 表示的是
表示的是