题目内容
将40g 10%的氢氧化钠溶液与100g 3.65%的盐酸混合,所得溶液中溶质的质量分数约为
- A.
 ×100%
×100% - B.
 ×100%
×100% - C.
 ×100%
×100% - D.
 ×100%
×100%
B
分析:根据氢氧化钠与盐酸反应的化学方程式中两物质的质量关系,可判断将40g 10%的氢氧化钠溶液与100g 3.65%的盐酸混合时,两物质恰好完全反应,反应后得到氯化钠溶液,由化学方程式求得生成氯化钠的质量、由质量守恒求得反应所得溶液的质量,即可列出所得溶液中溶质的质量分数的算式.
解答:40g 10%的氢氧化钠溶液中含氢氧化钠质量40g×10%=4g,100g 3.65%的盐酸中含HCl的质量=100g×3.65%=3.65g,根据反应的化学方程式,两溶液混合时恰好完全反应,反应后得到氯化钠溶液;
设反应生成氯化钠的质量为x
NaOH+HCl═NaCl+H2O
40 36.5 58.5
4g 3.65g x
 =
=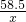 x=5.85g
x=5.85g
所得溶液中溶质的质量分数= ×100%=
×100%= ×100%
×100%
故选B.
点评:根据反应的化学方程式中物质的质量比,判断反应物是否完全反应,是解答此类反应物质量均已知类问题的前提.
分析:根据氢氧化钠与盐酸反应的化学方程式中两物质的质量关系,可判断将40g 10%的氢氧化钠溶液与100g 3.65%的盐酸混合时,两物质恰好完全反应,反应后得到氯化钠溶液,由化学方程式求得生成氯化钠的质量、由质量守恒求得反应所得溶液的质量,即可列出所得溶液中溶质的质量分数的算式.
解答:40g 10%的氢氧化钠溶液中含氢氧化钠质量40g×10%=4g,100g 3.65%的盐酸中含HCl的质量=100g×3.65%=3.65g,根据反应的化学方程式,两溶液混合时恰好完全反应,反应后得到氯化钠溶液;
设反应生成氯化钠的质量为x
NaOH+HCl═NaCl+H2O
40 36.5 58.5
4g 3.65g x
 =
=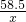 x=5.85g
x=5.85g所得溶液中溶质的质量分数=
 ×100%=
×100%= ×100%
×100%故选B.
点评:根据反应的化学方程式中物质的质量比,判断反应物是否完全反应,是解答此类反应物质量均已知类问题的前提.

练习册系列答案
相关题目
 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:
现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算: “世界环境日:活动中,某小组对生产及生活污水进行了探究。
“世界环境日:活动中,某小组对生产及生活污水进行了探究。