题目内容
实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6 g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.
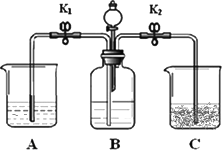
①10.6 g纯碱的物质的量是________;如果加入足量的硫酸,反应中得到的二氧化碳的物质的量是多少?请写出化学反应方程式,并列式计算,写出计算过程:________.
②烧杯C中并没有明显现象,为了证明B中的确产生了CO2,现将C中悬浊液进行固液分离,该分离操作除烧杯外,还需用到的玻璃仪器有________(写名称).过滤后滤液能使酚酞试液变红,则滤液中的主要溶质是________,该现象________(填写“能”或“不能”)说明产生了CO2.
③上述过滤后的滤渣可能存在Ca(OH)2和CaCO3.某同学为证明该两种物质同时存在,在一支试管中取少量样品,经过两个步骤完成了检验.若所有检验实验均在该支试管中进行,请完成实验报告:
④实验一段时间后,关闭开关K2打开K1,见到B中液体将会压入到烧杯A中,实验中可能见到不同的现象,请完成下表:

答案:
解析:
解析:
|
①0.1 mol Na2CO3+H2SO4→Na2SO4+H2O+CO2↑ 设:得到CO2气体的物质的量为x mol x=0.1 mol ②玻璃棒、漏斗 Ca(OH)2 不能 ③取样加水溶解并滴加酚酞,溶液变红色 Ca(OH)2 继续滴加盐酸,有气泡产生 CaCO3 ④(16)Na2CO3、Na2SO4 Na2CO3+Ca(OH)2→CaCO3↓+2NaOH H2SO4、Na2SO4 H2SO4+Ca(OH)2→CaSO4+2H2O |

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目

 (2012?普陀区二模)实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.
(2012?普陀区二模)实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.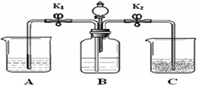 实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.
实验室用下图装置进行碳酸钠的性质实验,烧杯A中是澄清石灰水并滴加了酚酞,C中是石灰乳.实验开始前,称取10.6g纯碱置于B中,关闭开关K1打开K2,并加入一定量的稀硫酸.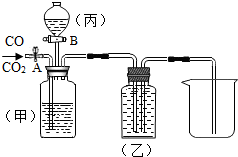 (2013?怀柔区二模)实验室用下图装置进行CO与CO2的分离和对比实验.其中甲瓶盛足量的NaOH溶液,乙瓶盛有澄清石灰水,分液漏斗(丙)盛稀硫酸.
(2013?怀柔区二模)实验室用下图装置进行CO与CO2的分离和对比实验.其中甲瓶盛足量的NaOH溶液,乙瓶盛有澄清石灰水,分液漏斗(丙)盛稀硫酸.