题目内容
用100g含杂质3.2%的生铁粉(杂质不参与反应),与质量分数为10%的稀硫酸恰好完全反应制硫酸亚铁。求消耗的稀硫酸质量。
解:设消耗稀硫酸的质量为x
 Fe + H2SO4 = FeSO4 + H2↑ (1分)
Fe + H2SO4 = FeSO4 + H2↑ (1分)
56 98
100g×(1-3.2%) x×10% (1分)
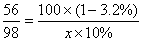
x = 1694g (1分)
答:消耗的稀硫酸质量为1694g。(设答正确1分)

练习册系列答案
相关题目
题目内容
用100g含杂质3.2%的生铁粉(杂质不参与反应),与质量分数为10%的稀硫酸恰好完全反应制硫酸亚铁。求消耗的稀硫酸质量。
解:设消耗稀硫酸的质量为x
 Fe + H2SO4 = FeSO4 + H2↑ (1分)
Fe + H2SO4 = FeSO4 + H2↑ (1分)
56 98
100g×(1-3.2%) x×10% (1分)
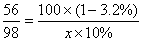
x = 1694g (1分)
答:消耗的稀硫酸质量为1694g。(设答正确1分)
