题目内容
 甲、乙学生在学习了“质量守恒定律”后,利用右图所示实验进行探究,以证明其它化学反应也遵守质量守恒定律.他们先使天平平衡,称出烧杯、小试管、药品的总质量,此时指针处于中间位置.然后将小试管里的药品倒入烧杯中,观察现象.待反应完全后,再次称量其总质量.请你与他们一起探究:
甲、乙学生在学习了“质量守恒定律”后,利用右图所示实验进行探究,以证明其它化学反应也遵守质量守恒定律.他们先使天平平衡,称出烧杯、小试管、药品的总质量,此时指针处于中间位置.然后将小试管里的药品倒入烧杯中,观察现象.待反应完全后,再次称量其总质量.请你与他们一起探究:
(1)甲同学在实验过程中可观察到的现象:①______;②______.
反应的化学方程式为:______.
乙同学在实验过程中可观察到的现象:①______;②______.
反应的化学方程式为:______.
(2)甲、乙两学生根据各自的实验虽然得出了不同的结论.但通过讨论他们得出化学反应前后______必然相等.
解:(1)甲同学在实验过程中发生的反应是氯化钡和硫酸钠反应生成硫酸钡沉淀,反应后物质的总质量不变,可观察到的现象①烧杯中有白色沉淀生成,;②天平保持平衡;反应的化学方程式为BaCl2+Na2S04=BaS04↓+2NaCl;
乙同学在实验过程中发生的反应是碳酸钠和盐酸生成二氧化碳气体,反应后锥形瓶内质量减少,可观察到的现象:①烧杯中有气泡生成,;②天平指针向右偏转;反应的化学方程式为:Na2C03+2HCl=2NaCl+H20+C02↑.
(2)甲同学与乙同学根据各自的实验现象得出了不同的结论的原因是甲同学的实验中没有漏掉反应物和生成物的质量,而乙同学的实验漏掉生成物中气体的质量,若改在密闭容器中进行也能验证质量守恒定律;这两个反应都是化学变化,化学反应的实质是分子破裂成原子,原子再重新组合成新的分子,所以反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,因此化学反应前后物质的质量是不发生变化的.
故答案为:(1)①烧杯内产生白色沉淀;②天平平衡;BaCl2+Na2SO4=BaSO4↓+2NaCl;
①烧杯内产生大量气体;②天平右侧下沉(天平不平衡);Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)物质的质量总和.
分析:(1)根据物质反应时生成物的状态和反应后锥形瓶内质量的变化分析;书写化学方程式时要注意反应物和生成物的化学式,并且不要忘记配平和生成物状态符号;
(2)根据质量守恒定律的适用范围分析结论:所有的化学变化都符合质量守恒定律;乙之所以天平不平衡的原因是反应中生成了气体的缘故.所以要想天平平衡,就必须要在密闭容器中进行.
点评:对于质量守恒定律的理解要注意时所用的物质的质量包括气体固体和液体,而气体容易被忽略,所以在设计验证质量守恒的实验时要考虑实验在密闭容器中进行.
乙同学在实验过程中发生的反应是碳酸钠和盐酸生成二氧化碳气体,反应后锥形瓶内质量减少,可观察到的现象:①烧杯中有气泡生成,;②天平指针向右偏转;反应的化学方程式为:Na2C03+2HCl=2NaCl+H20+C02↑.
(2)甲同学与乙同学根据各自的实验现象得出了不同的结论的原因是甲同学的实验中没有漏掉反应物和生成物的质量,而乙同学的实验漏掉生成物中气体的质量,若改在密闭容器中进行也能验证质量守恒定律;这两个反应都是化学变化,化学反应的实质是分子破裂成原子,原子再重新组合成新的分子,所以反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,因此化学反应前后物质的质量是不发生变化的.
故答案为:(1)①烧杯内产生白色沉淀;②天平平衡;BaCl2+Na2SO4=BaSO4↓+2NaCl;
①烧杯内产生大量气体;②天平右侧下沉(天平不平衡);Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)物质的质量总和.
分析:(1)根据物质反应时生成物的状态和反应后锥形瓶内质量的变化分析;书写化学方程式时要注意反应物和生成物的化学式,并且不要忘记配平和生成物状态符号;
(2)根据质量守恒定律的适用范围分析结论:所有的化学变化都符合质量守恒定律;乙之所以天平不平衡的原因是反应中生成了气体的缘故.所以要想天平平衡,就必须要在密闭容器中进行.
点评:对于质量守恒定律的理解要注意时所用的物质的质量包括气体固体和液体,而气体容易被忽略,所以在设计验证质量守恒的实验时要考虑实验在密闭容器中进行.

练习册系列答案
相关题目


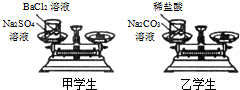 (2006?朝阳区一模)甲、乙学生在学习了“质量守恒定律”后,利用右图所示实验进行探究,以证明其它化学反应也遵守质量守恒定律.他们先使天平平衡,称出烧杯、小试管、药品的总质量,此时指针处于中间位置.然后将小试管里的药品倒入烧杯中,观察现象.待反应完全后,再次称量其总质量.请你与他们一起探究:
(2006?朝阳区一模)甲、乙学生在学习了“质量守恒定律”后,利用右图所示实验进行探究,以证明其它化学反应也遵守质量守恒定律.他们先使天平平衡,称出烧杯、小试管、药品的总质量,此时指针处于中间位置.然后将小试管里的药品倒入烧杯中,观察现象.待反应完全后,再次称量其总质量.请你与他们一起探究: