题目内容
 某校兴趣小组同学对氢氧化钠和稀盐酸发生中和反应的有关问题,进行了如下实验.(以下2小题选做1题,若两题都做,则以第(1)小题记分)
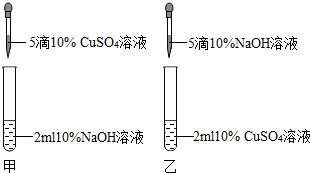
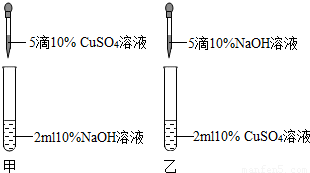
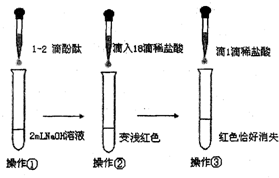
某校兴趣小组同学对氢氧化钠和稀盐酸发生中和反应的有关问题,进行了如下实验.(以下2小题选做1题,若两题都做,则以第(1)小题记分)(1)甲同学为了证明氢氧化钠和稀盐酸能够发生化学反应,设计并完成了如图所示实验.
回答问题:操作①观察到的现象是:
变红
变红
,操作②的过程中要不断振荡
振荡
,(填操作名),操作③后管内溶液pH的一定等于7不是
不是
.(填是或不是)(2)乙同学也设计完成了另一个实验,证明氢氧化钠和稀盐酸能够发
生化学反应.并伴随能量变化,在盛2mL氢氧化钠溶液的试管里,用胶头滴管慢慢滴入稀盐酸,每滴2滴测一次pH直到盐酸过量.插入温度计测试反应后溶液温度.
①实验中溶液的pH发生怎样的变化?
由大于7逐渐变到小于7
由大于7逐渐变到小于7
.②氢氧化钠和稀盐酸反应后溶液温度
升高
升高
.(升高或降低或几乎不变)③你认为甲、乙两位同学的实验中,哪一位同学的实验能充分证明氢氧化钠和盐酸发生了反应?
乙
乙
.分析:(1)根据酚酞在酸碱性溶液中的变化情况判断.
(2)根据中和反应放热解答.
(2)根据中和反应放热解答.
解答:解:(1)氢氧化钠呈碱性,能使无色酚酞试液变红,加入盐酸的过程中要不断振荡,使盐酸与氢氧化钠充分反应,防止局部酸液过量,酚酞在中性或酸性溶液中都显无色,当红色消失时并不能说明盐酸与氢氧化钠恰好完全反应,反应后管内溶液pH不一定等于7.
(2)①开始溶液为氢氧化钠溶液,呈碱性,pH大于7,随着盐酸的不断加入,碱性减弱,当恰好完全反应时呈中性,pH=7,当盐酸过量时,pH小于7
②氢氧化钠和稀盐酸反应后溶液温度 升高.
③你认为甲、乙两位同学的实验中,乙同学的实验能充分证明氢氧化钠和盐酸发生了反应
故答案为:(1)变红 振荡 不是
(2)由大于7逐渐变到小于7 升高 乙
(2)①开始溶液为氢氧化钠溶液,呈碱性,pH大于7,随着盐酸的不断加入,碱性减弱,当恰好完全反应时呈中性,pH=7,当盐酸过量时,pH小于7
②氢氧化钠和稀盐酸反应后溶液温度 升高.
③你认为甲、乙两位同学的实验中,乙同学的实验能充分证明氢氧化钠和盐酸发生了反应
故答案为:(1)变红 振荡 不是
(2)由大于7逐渐变到小于7 升高 乙
点评:明确中和反应指示剂的作用及热量变化分析解答.

练习册系列答案
相关题目