题目内容
2.目前,农业上使用最多的氮肥主要有尿素、硝酸铵和碳酸氢铵等,其中硝酸铵的生产原理是利用氨催化氧化得到的硝酸,再跟氨反应生产硝酸铵,基本流程如下:
已知:①上述流程图中A、B、C均为气体,其中A、B为单质且A的相对分子质量为28,C为含有A组成元素的化合物;氨与氧气反应的条件是高温、催化剂.
②在化学反应中,只要有物质所含元素的化合价发生了变化的反应就是氧化还原反应.例如:2Na+2H2O═2NaOH+H2↑,反应前后,Na元素、H元素的化合价分别发生了变化,该反应是氧化还原反应.
请回答下列问题:
(1)写出A、C两种物质的化学式:A为N2;C为NO.
(2)NH3和O2反应的化学方程式为4NH3+5O2$\frac{\underline{\;催化剂\;}}{高温}$4NO+6H2O
(3)上述流程图的5个反应中有4个属于氧化还原反应.
分析 根据A、B、C均为气体,A、B反应产生氨气,其中A、B为单质且A的相对分子质量为28,其中A为氮气,B为氢气,C为含有A组成元素的化合物,因此C为一氧化氮,然后根据信息完成相关的问题.
解答 解:(1)A、B、C均为气体,A、B反应产生氨气,其中A、B为单质且A的相对分子质量为28,其中A为氮气,B为氢气,C为含有A组成元素的化合物,因此C为一氧化氮;故填:N2;NO;
(2)氨与氧气反应生成一氧化氮和水,反应条件是高温、催化剂,故方程式为:4NH3+5O2$\frac{\underline{\;催化剂\;}}{高温}$4NO+6H2O;
(3)在化学反应中,只要有物质所含元素的化合价发生了变化的反应就是氧化还原反应,其中氮气和氢气的反应,氨气和氧气的反应,一氧化碳和氧气的反应都有单质的反应,因此元素的化合价一定变;二氧化氮和水反应产生一氧化氮和硝酸,氮元素的化合价也发生了改变,只有氨气和硝酸的反应没有元素化合价的改变,不属于氧化还原反应,因此属于氧化还原反应的有4个;故填:4.
点评 本题属于信息题的考查,考查了化学反应及化学肥料的知识,完成此题,可以依据已有的知识进行,能够考查学生运用知识的能力.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
13.下列所示的四个图象,能正确反映对应变化关系的是( )
| A. |  电解水 | |
| B. |  向两份完全相同的稀盐酸中分别加入锌粉和铁粉 | |
| C. |  加热一定质量的高锰酸钾 | |
| D. |  向一定量的氢氧化钠溶液中加水稀释 |
10.只用一种试剂可以区分(NH4)2SO4、NH4Cl、K2SO4三种无色溶液,这种试剂是( )
| A. | AgNO3溶液 | B. | Ba(OH)2溶液 | C. | NaOH溶液 | D. | 盐酸 |
7.小华同学为母亲过生日,下列庆祝活动中发生了化学变化的是( )
| A. | 编制花环 | B. | 榨取果汁 | C. | 点燃蜡烛 | D. | 切分蛋糕 |
14.下列图象不能正确反映对应变化关系的是( )
| A. | 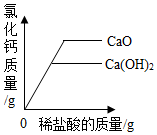 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量 | |
| B. | 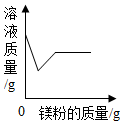 向一定质量氯化亚铁和氯化铝的混合溶液至加入镁粉至过量 | |
| C. |  向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量 | |
| D. |  向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量 |
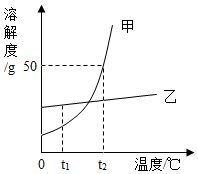 如图为甲和乙两种固体物质的溶解度曲线.回答下列问题:
如图为甲和乙两种固体物质的溶解度曲线.回答下列问题: