题目内容
水通电生成氢气和氧气,其反应的化学方程式为:2H2O
2H2↑+O2↑.
试计算:
(1)该反应中H2O、H2、O2微粒的个数比为 ;
(2)该反应中H2O、H2、O2的质量比为 ;
(3)如果18g水通电全部分解,可得到氧气16g,同时得到氢气 g;
(4)如果72g水通电全部分解,可得到氢气 g;
(5)要得到1g氢气,需要分解水的质量是 g.
| ||
试计算:
(1)该反应中H2O、H2、O2微粒的个数比为
(2)该反应中H2O、H2、O2的质量比为
(3)如果18g水通电全部分解,可得到氧气16g,同时得到氢气
(4)如果72g水通电全部分解,可得到氢气
(5)要得到1g氢气,需要分解水的质量是
考点:化学方程式的概念、读法和含义,根据化学反应方程式的计算
专题:化学用语和质量守恒定律
分析:根据化学方程式中各物质的质量比及分子个数比进行解答.
解答:解:根据反应的化学方程式2H2O
2H2↑+O2↑可知,该反应中H2O、H2、O2微粒的个数比为2:2:1;H2O、H2、O2的质量比为9:1:8,因此:
(1)该反应中H2O、H2、O2微粒的个数比为2:2:1;
(2)该反应中H2O、H2、O2的质量比为9:1:8;
(3)因为氧气与氢气的质量比为8:1,氧气为16g,故氢气的质量为:16g÷8=2g;
(4)因为该反应中H2O、H2的质量比为9:1,故可得到氢气质量为72g÷9=8g;
(5)因为该反应中H2O、H2的质量比为9:1,故需要分解水的质量是1g×9=9g.
故答案为:(1)2:2:1;
(2)9:1:8;
(3)2;
(4)8;
(5)9.
| ||
(1)该反应中H2O、H2、O2微粒的个数比为2:2:1;
(2)该反应中H2O、H2、O2的质量比为9:1:8;
(3)因为氧气与氢气的质量比为8:1,氧气为16g,故氢气的质量为:16g÷8=2g;
(4)因为该反应中H2O、H2的质量比为9:1,故可得到氢气质量为72g÷9=8g;
(5)因为该反应中H2O、H2的质量比为9:1,故需要分解水的质量是1g×9=9g.
故答案为:(1)2:2:1;
(2)9:1:8;
(3)2;
(4)8;
(5)9.
点评:本题主要考查根据化学方程式求各物质的质量比及分子个数比.

练习册系列答案
相关题目
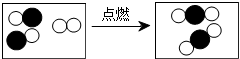 如图示意图形象地表示了某化学反应前后分子的变化.其中
如图示意图形象地表示了某化学反应前后分子的变化.其中 表示氧原子,
表示氧原子, 表示碳原子,则该反应的化学方程式为:
表示碳原子,则该反应的化学方程式为: A、B、C、D、E、F为初中化学常见物质,它们之间的转化如图所示,A是固体物质,C是气体,请回答下列问题:
A、B、C、D、E、F为初中化学常见物质,它们之间的转化如图所示,A是固体物质,C是气体,请回答下列问题: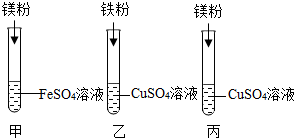 某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案
某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案