题目内容
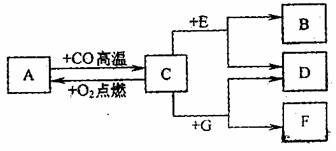
某化学兴趣小组对某铜锌合金样品进行探究实验。称取样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示。求:
(1)铜锌合金汇中,Zn的质量分数是 65%
(2)所用稀硫酸溶液中溶质的质量分数是多少?
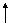 解:设反应中消耗稀硫酸溶液中溶质的质量为X,
解:设反应中消耗稀硫酸溶液中溶质的质量为X,
Zn + H2SO4 === ZnSO4 + H2
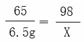 65 98
65 98
6.5g X
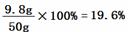 解得:X = 9.8g
解得:X = 9.8g
所以,所用稀硫酸溶液中溶质的质量分数为:
海南石碌铁矿,其矿石主要成分为Fe2O3。炼铁的化学方程式为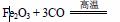
 请计算:某铁矿石,其中含Fe2O3 的质量为16t,理论上可以炼出铁的质量为多
请计算:某铁矿石,其中含Fe2O3 的质量为16t,理论上可以炼出铁的质量为多
少?

练习册系列答案
相关题目
某腐蚀印刷电路板的废液中含有CuCl2和FeCl2,为了分析该废液的组成,取1 000 g废液,设计如下实验方案进行探究:

实验过程中加入废铁屑的质量、析出Cu的质量的数据记录如下表:
| 废铁屑的质量/g | 20 | 40 | 60 | 80 |
| 析出Cu的质量/g | 12.8 | 25.6 | 32 | 32 |
(注:废铁屑中的杂质不溶于废液也不与废液反应,不考虑过滤中的损失。)
(1)1 000 g废液与足量废铁屑完全反应,析出Cu的质量为 。
(2)废铁屑中单质Fe的质量分数为 。
(3)计算1 000 g废液中CuCl2的质量分数。(写出计算过程,结果保留小数点后一位)
(4)1 000 g废液中FeCl2的质量分数为 。(结果保留小数点后一位)